题目内容
某学习小组的同学在做碳酸钠溶液和澄清石灰水反应的实验后,将反应后的浑浊液进行过滤,得到澄清的滤液,对于滤液的组成同学们做出如下猜想:
(1)【猜想与假设】大家一致认为滤液中一定有氢氧化钠,生成氢氧化钠的化学方程式是________;小明猜想还可能有氢氧化钙,小丽猜想还可能有氢氧化钙和碳酸钠,你还能做出的猜想是________.
(2)【活动与探究】请你设计一个实验方案验证你的猜想.
| 实验步骤 | 实验现象 | 实验结论 |
解:(1)碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸钠和氢氧化钙反应时,可能存在碳酸钠过量,也可能存在氢氧化钙过滤,故填:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓,可能有碳酸钠;
(2)碳酸钠能与盐酸反应生成二氧化碳气体,可以向反应后的滤液中加入过量的稀盐酸,观察到气泡产生,说明猜想成立,故填:
(3)2NaOH+H2SO4=Na2SO4+2H2O,Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,根据反应的化学方程式可以看出,反应后所得的溶液中溶质是硫酸钠,设生成硫酸钠的质量为x
H2SO4------Na2SO4
98 142
100g×9.8% x
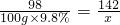 x=14.2g
x=14.2g
故填:14.2.
分析:根据已有的知识进行分数,碳酸钠与氢氧化钙反应时,可能存在物质过量的情况,要设计实验证明物质的存在,可以依据物质的性质进行,根据反应的化学方程式即可计算出生成的硫酸钠的质量,据此解答即可.
点评:本题考查了反应后溶液中物质成分的推断,完成此题,可以依据物质的性质进行,进行化学方程式计算时,可以依据硫酸与硫酸钠的质量比为定值进行.
(2)碳酸钠能与盐酸反应生成二氧化碳气体,可以向反应后的滤液中加入过量的稀盐酸,观察到气泡产生,说明猜想成立,故填:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入足量稀盐酸 | 有气体产生 | 猜想成立 |
H2SO4------Na2SO4
98 142
100g×9.8% x
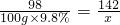 x=14.2g
x=14.2g故填:14.2.
分析:根据已有的知识进行分数,碳酸钠与氢氧化钙反应时,可能存在物质过量的情况,要设计实验证明物质的存在,可以依据物质的性质进行,根据反应的化学方程式即可计算出生成的硫酸钠的质量,据此解答即可.
点评:本题考查了反应后溶液中物质成分的推断,完成此题,可以依据物质的性质进行,进行化学方程式计算时,可以依据硫酸与硫酸钠的质量比为定值进行.

练习册系列答案
相关题目
(10分)(2012?宁夏)某学习小组的同学在做碳酸钠溶液和澄清石灰水反应的实验后,将反应后的浑浊液进行过滤,得到澄清的滤液,对于滤液的组成同学们做出如下猜想:
【猜想与假设】大家一致认为滤液中一定有氢氧化钠,生成氢氧化钠的化学方程式是 _________ ;小明猜想还可能有氢氧化钙,小丽猜想还可能有氢氧化钙和碳酸钠,你还能做出的猜想是 _________ .
【活动与探究】请你设计一个实验方案验证你的猜想.
| 实验步骤 | 实验现象 | 实验结论 |
| | | |
(2) _________ .
某学习小组的同学在做碳酸钠溶液和澄清石灰水反应的实验后,将反应后的浑浊液进行过滤,得到澄清的滤液,对于滤液的组成同学们做出如下猜想:
【猜想与假设】大家一致认为滤液中一定有氢氧化钠,生成氢氧化钠的化学方程式是 ;小明猜想还可能有氢氧化钙,小丽猜想还可能有氢氧化钙和碳酸钠,你还能做出的猜想是 .
【活动与探究】请你设计一个实验方案验证你的猜想.
| 实验步骤 | 实验现象 | 实验结论 |
【反思与提高】请你总结归纳出碳酸钠的两条化学性质:
(1) ;
(2) ; .
某学习小组的同学在做碳酸钠溶液和澄清石灰水反应的实验后,将反应后的浑浊液进行过滤,得到澄清的滤液,对于滤液的组成同学们做出如下猜想:
【猜想与假设】大家一致认为滤液中一定有氢氧化钠,生成氢氧化钠的化学方程式是______;小明猜想还可能有氢氧化钙,小丽猜想还可能有氢氧化钙和碳酸钠,你还能做出的猜想是______.
【活动与探究】请你设计一个实验方案验证你的猜想.
【反思与提高】请你总结归纳出碳酸钠的两条化学性质:
(1)______;
(2)______.
【猜想与假设】大家一致认为滤液中一定有氢氧化钠,生成氢氧化钠的化学方程式是______;小明猜想还可能有氢氧化钙,小丽猜想还可能有氢氧化钙和碳酸钠,你还能做出的猜想是______.
【活动与探究】请你设计一个实验方案验证你的猜想.
| 实验步骤 | 实验现象 | 实验结论 |
(1)______;
(2)______.