题目内容
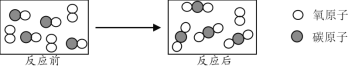
【题目】A、B、C、D、E是初中化学中常见的五种物质,A、E是黑色固体,B、C均为无色气体,且单质B是空气的主要成分之一,实验室常用含D的物质与稀盐酸反应制取C,它们之间的反应及转化关系如图所示。

(1)D的名称是__________,E的相对分子质量是__________。
(2)反应②的现象是____________。
(3)反应④的方程式是___________。
【答案】碳酸钙 80 有红色固体产生 CaCO3+2HCl=CaCl2+H2O+CO2↑(或CaCO3![]() CaO+CO2↑)
CaO+CO2↑)
【解析】
B为无色气体,且单质B是空气的主要成分之一,B可能是氧气;A是黑色固体,A与B(氧气)能转化为C,实验室常用含D的物质与稀盐酸反应制取C,碳是黑色固体,碳在氧气中燃烧生成二氧化碳,实验室常用大理石(含碳酸钙)与稀盐酸反应制取二氧化碳, A可能是碳,C可能是二氧化碳,D可能是碳酸钙,二氧化碳与氢氧化钙反应生成碳酸钙和水;E是黑色固体,A(碳)与E能转化为C(二氧化碳),氧化铜是黑色固体,碳与氧化铜在高温条件下生成铜和二氧化碳,E可能为氧化铜。代入框图,猜想合理。
(1)D的名称是碳酸钙,E是氧化铜,其相对分子质量是64+16×2=80;
(2)反应②是碳与氧化铜在高温条件下生成铜和二氧化碳,现象是有红色固体产生;
(3)反应④是碳酸钙转化为二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,碳酸钙高温条件下生成氧化钙和二氧化碳,化学方程式分别是CaCO3+2HCl=CaCl2+H2O+CO2↑,CaCO3![]() CaO+CO2↑。
CaO+CO2↑。

【题目】某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了11.4g钢样品,投入装有20.0g稀盐酸(足量)的烧杯中(烧杯质量也为20.0g)。在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
反应时间 | t0 | t1 | t2 | t3 |
烧杯和药品的质量(克) | 51.4 | 51.2 | 51.0 | 51.0 |
(1)反应中产生氢气____________克。
(2)这种钢样品中铁的质量分数是______________?(精确到0.1﹪)