题目内容
【题目】现有含有7.4gCa(OH)2的石灰乳,请按下面要求计算:
(1)向上述石灰乳中通入CO2,当二者恰好完全反应生成碳酸钙时,通入CO2的质量是多少克?(写出计算过程)______
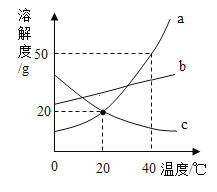
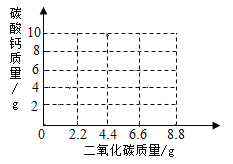
(2)已知反应![]() 。请在图中画出通入二氧化碳过程中碳酸钙质量的变化曲线。______
。请在图中画出通入二氧化碳过程中碳酸钙质量的变化曲线。______
(3)另取一定量的石灰乳,通入一段时间的CO2,反应物与生成物的质量如下表:
物质 | Ca(OH)2 | CO2 | CaCO3 | X | H2O |
质量/g | 14.8 | 13.2 | 10 | a | 1.8 |
则a=_____________;该反应的化学方程式为________________。
【答案】4.4g  16.2
16.2 ![]()
【解析】
(1)解:设当二者恰好完全反应生成碳酸钙时,通入CO2的质量为x。

![]() ,解得x=4.4g
,解得x=4.4g
二者恰好究全反应生成碳酸钙时,通入CO2的质量为4.4g;
(2)通入二氧化碳和氢氧化钙反应生成碳酸钙,碳酸钙的质量增加,当通入4.4g二氧化碳时,正好完全反应,碳酸钙质量达到最大;之后碳酸钙又和水和二氧化碳反应生成碳酸氢钙,则碳酸钙的质量逐渐减小,直至变为0;故碳酸钙的质量变化曲线为如图所示:

(3)氢氧化钙和二氧化碳反应生成碳酸钙,碳酸氢钙和水,由质量守恒定律可知,X(碳酸氢钙)的质量为14.8g+13.2g-10g-1.8g=16.2g,所以a=16.2g;
反应的化学方程式为![]() 。
。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目