题目内容
【题目】某小组进行了如下实验,请回答下列问题
序号 | 甲 | 乙 | 丙 |
实验 |
|
|
a,c为干燥的紫色石蕊试纸 b,d为湿润的紫色石蕊试纸 |
(1)甲实验的目的是______。
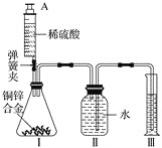
(2)乙实验探究铁,铜、银的金属活动性顺序,为了达到实验目的,金属X是______,能得出金属活动性Fe>Cu>Ag的实验现象是______,化学反应方程式是______。
(3)丙实验,说明二氧化碳密度大于空气且能与水反应的现象是______。
【答案】比较高锰酸钾在水和汽油中溶解情况 铜 A中无明显现象,B中有银白色固体析出,溶液颜色由无色变为蓝色 Cu+2AgNO3=Cu(NO3)2+2Ag a、c不变色,d比b先变红
【解析】
二氧化碳能与水反应生成碳酸,排在越后的金属越容易,也越先从它们的化合物中被置换出来;排在越前的金属越容易,也越先把其他化合物中的金属置换出来。
(1)在两支试管中只有溶剂不同,其他相同,说明实验目的是比较高锰酸钾在水和汽油中溶解情况。
(2)在验证三种金属活动性强弱时,通常采取“三取中”的方法,即取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应,故为了达到实验目的,金属X是铜;能得出金属活动性Fe>Cu>Ag的实验现象是A中无明显现象,B中有银白色固体析出,溶液颜色由无色变为蓝色,说明铜的金属活动性比铁弱,比银强,化学方程式为![]() 。
。
(3)二氧化碳不能使干燥的紫色石蕊试纸变色;二氧化碳能与水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,能使湿润的紫色石蕊试纸变红色;a、c不变色,d比b先变红,能说明二氧化碳密度大于空气且能与水反应的现象。

 阅读快车系列答案
阅读快车系列答案【题目】在一次聚餐中,同学们对燃料“固体酒精”产生了兴趣,于是对该固体酒精的成分进行探究。
(查阅资料)(1)固体酒精由酒精、氯化钙和氢氧化钠按一定质量比例混制成。
(2)氯化钙溶液呈中性,碳酸钠溶液呈碱性。
(提出问题)(1)酒精中是否含有碳元素?
(2)该固体酒精中的氢氧化钠是否变质?
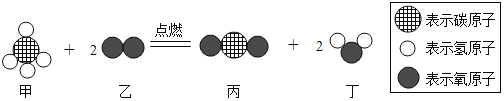
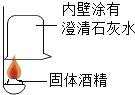
(实验探究)(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论,此结论_____(填“合理”或“不合理”)
(2)取少量该固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,该气体是_____。
(实验结论)分析实验并结合资料得出氢氧化钠已变质。
(拓展实验)为进一步确定氢氧化钠的变质程度,小北同学做了以下实验:
实验方案 | 实验现象 | 实验结论 |
取烧杯中上层清液于试管中,加入几滴酚酞溶液 | 溶液变红 | 清液中有氢氧化钠 |
另取烧杯中上层清液于试管中,加入澄清石灰水溶液 | 产生_____ | 清液中有碳酸钠 |
(1)有同学认为小北的实验不能证明清液中一定有氢氧化钠,理由是_____。
(2)该同学另取烧杯中上层清液,加入足量的氯化钙溶液充分反应,有白色沉淀生成,反应后滴加酚酞溶液,溶液变红,加入足量氯化钙溶液的目的是_____,写出生成沉淀的化学方程式:_____。
(3)实验结论:固体酒精中氢氧化钠的变质程度是_____(填“完全变质”或者“部分变质”)
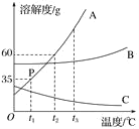
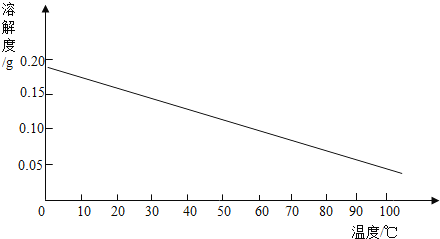
【题目】物质的溶解性受到各种因素的影响,请根据下列信息回答问题:
表一:常温下,一些物质在水中的溶解度
Ba(NO3)2 | BaCl2 | AgCl | AgNO3 | |
水 | 9.2g | 33.3g | 0.00015g | 170.0g |
表二:常温下,一些物质在乙醇中的溶解度
Ba(NO3)2 | BaCl2 | NaOH | NaCl | Ca(NO3)2 | CaCl2 | |
乙醇 | 0.002g | 4.1g | 14.7g | 0.07g | 33.9g | 20.5g |
(1)表一、表二数据说明物质的溶解性受到_____等因素的影响。
(2)常温下,40g水中加入2gBa(NO3)2固体,充分溶解,得到溶液质量为_____g。
(3)酸、碱、盐在溶液中发生复分解反应的条件是有沉淀析出、或有气体放出、或有水生成。请回答
①表一中物质在水中发生复分解反应的化学方程式_____。
②表二中物质在乙醇中发生复分解反应的化学方程式_____。从微观的角度看,溶液中减少的微粒是_____(写微粒符号)。
【题目】兴趣小组同学为了测定某中碳酸钙的质量分数,称取25.0g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数 | 第1次 | 第2次 | 第3次 | 第4次 |
剩余固体质量(g) | 21.6 | 19.2 | 16.2 | 16.2 |
试计算:
(1)完全反应后生成二氧化碳的质量是__g。
(2)求珍珠粉中碳酸钙的质量分数。(写出计算过程)__________.