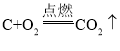题目内容
【题目】人类的生产生活离不开金属。
(1)日常生活用品大多用到了金属材料,现在年产量最高的金属是________。
(2)铝制品具有较好的抗腐蚀性能是因为________ (用化学方程式表示)。
(3)现有镁、铁、银的混合物若干放入硫酸铜溶液中,充分反应后过滤,向滤渣中加入稀盐酸,观察到有气泡冒出,则滤渣中一定含有________。
(4)现有一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。
①若所加硫酸铜溶液不足,则滤液中一定含有的溶质为________(填化学式)。
②若所加硫酸铜溶液过量,则该镀锌铁片中铁与锌的质量最简比为________。
【答案】铁(Fe) ![]() Fe、Cu和Ag FeSO4和ZnSO4 112:13
Fe、Cu和Ag FeSO4和ZnSO4 112:13
【解析】
(1)现在年产量最高的金属是铁;
(2)铝制品具有较好的抗腐蚀性能是因为铝与空气中氧气反应生成致密的氧化铝薄膜,阻碍反应进一步发生,化学方程式为4Al+3O2═2Al2O3;
(3)镁、铁、银的混合物若干放入硫酸铜溶液中,镁先与硫酸铜反应生成铜和硫酸镁,若硫酸铜剩余,然后铁再与硫酸铜反应生成铜和硫酸亚铁。充分反应后过滤,向滤渣中加入稀盐酸有气泡冒出,说明滤渣中一定含有银、铜和铁,若镁过量则含有镁;
(4)在金属活动性顺序表中只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,位于氢前面的金属能置换出酸中的氢。金属活动性由强至弱分别为锌>铁>铜,所以锌先和硫酸铜反应生成硫酸锌和铜,若硫酸铜剩余,然后铁再与硫酸铜反应生成铜和硫酸亚铁,反应的方程式分别为![]() ;
;![]() ;锌和硫酸铜反应固体质量减少,铁和硫酸铜反应固体质量增加,可知一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。最终的滤渣质量大于加入的固体质量,所以锌一定反应完全,铁一定参与反应。
;锌和硫酸铜反应固体质量减少,铁和硫酸铜反应固体质量增加,可知一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。最终的滤渣质量大于加入的固体质量,所以锌一定反应完全,铁一定参与反应。
①若所加硫酸铜溶液不足,则铁剩余,滤液中一定含有的溶质为FeSO4和ZnSO4。
②若所加硫酸铜溶液过量,则
设该镀锌铁片中锌的质量为![]() ,则铁的质量为6.25g-
,则铁的质量为6.25g-![]() ,
,
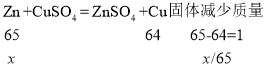
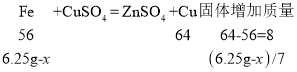
根据反应可知总质量增加量=过滤后的滤渣的质量-镀锌铁片的质量,可得
![]()
解得:![]()
则铁的质量为6.25g-0.65g=5.6g
则该镀锌铁片中铁与锌的质量最简比为5.6g:0.65g=112:13。

 阅读快车系列答案
阅读快车系列答案