题目内容
胃酸过多是常见的胃病.下面是甲、乙两种常见胃药的说明摘要.
甲:①白色结晶状粉末,受热可缓缓分解;②能溶于水,水溶液呈弱碱性;灼烧时火焰为黄色;③遇酸及酸性药物则产生二氧化碳;④患者服用过量,可能引起胃胀气,甚至有引起胃溃疡穿孔的危险.
乙:①与胃酸是中和作用缓慢而持久,可维持3~4小时;②凝胶本身覆盖于溃疡面上,具有保护作用;③可溶于稀酸或氢氧化钠溶液中.
(1)请你推测,甲中含有的主要化学成份是______(填化学式);乙中含有的主要化学成份是______(填化学式).
(2)试写出甲中含有的主要化学成份引起胃胀气反应的离子方程式:______.
(3)三硅酸镁Mg2Si3O8?nH2O也是常用胃药,被用来治疗胃溃疡,是因为该物质不溶于水,服用后中和胃酸作用持久.把三硅酸镁改写成氧化物形式为:______.写出它中和胃酸(胃酸的主要成分是HCl)的化学方程式______.
(4)目前一种新型抗酸剂能迅速改善和缓解胃酸过多的症状,它主要由碳酸镁、氢氧化镁和氢氧化铝组成(说明:Mg(OH)2在高温下分解为MgO).现按如下步骤测定药剂中三种主要成分的配比:
①取药剂样品,研磨后,加入50mL3.6mol?L-1盐酸,正好完全反应并收集得到标准状况下224mL气体
②过滤,弃去其中不溶性物质(其余成分不参与反应)
③取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4g.
则该药剂中三种主要成分的物质的量之比为n(MgCO3):n(Mg(OH)2):n(Al(OH)3)=______.
解:
(1)遇酸及酸性药物则产生二氧化碳,说明含有碳酸根离子或碳酸氢根离子,水溶液呈弱碱性,说明是强碱弱酸盐,灼烧时火焰为黄色,说明含有钠离子,白色结晶状粉末,受热可缓缓分解,碳酸钠不会分解,所以只能是碳酸氢钠;可溶于稀酸或氢氧化钠溶液中,该物质是一种两性碱,凝胶本身覆盖于溃疡面上,具有保护作用,说明该物质遇水会生成胶状物质,所以该物质是氢氧化铝,故答案为:NaHCO3;Al(OH)3;
(2)碳酸氢钠和盐酸的反应实质就是碳酸氢根离子和氢离子会生成水的反应,故答案为:HCO3-+H+═H2O+CO2↑;
(3)镁元素显+2价,硅元素显+4价,氢元素显+1价,氧元素显-2价,氧化物中只有氧和另一种元素,故答案为:2MgO?3SiO2?nH2O;
三硅酸镁和盐酸反应生成氯化镁、硅酸和水,故答案为:Mg2Si3O8?nH2O+4HCl=2MgCl2+3H2SiO3↓+(n-1)H2O;
(4)标准状况下224mL气体的物质的量是: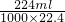 =0.01mol,
=0.01mol,
设生成0.01mol的二氧化碳需要碳酸镁物质的量是x,消耗盐酸物质的量是y,生成氯化镁物质的量是z,
MgCO3+2HCl=MgCl2+H2O+CO2↑
1 2 1 1
x y z 0.01
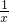 =
= =
= =
=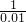
x=0.01mol y=0.02mol z=0.01mol
MgCl2+2NaOH=2NaCl+Mg(OH)2↓ Mg(OH)2 MgO+H2O
MgO+H2O
从方程式中可以看出氧化镁的物质的量和氯化镁的物质的量是相当的,
氧化镁物质的量: =0.06mol,所以氯化镁物质的量也是0.06mol;碳酸镁生成0.01mol的氯化镁,所以氢氧化镁生成0.05mol的氯化镁,
=0.06mol,所以氯化镁物质的量也是0.06mol;碳酸镁生成0.01mol的氯化镁,所以氢氧化镁生成0.05mol的氯化镁,
设生成0.05mol的氯化镁需要氢氧化镁m,消耗盐酸n,
Mg(OH)2+2HCl=MgCl2+2H2O
1 2 1
m n 0.05mol
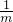 =
=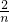 =
=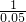
m=0.05mol n=0.1mol
所以与氢氧化铝反应的盐酸物质的量是: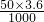 -0.1-0.02=0.06mol,
-0.1-0.02=0.06mol,
Al(OH)3+3HCl=AlCl3+3H2O,从方程式中可以看出氢氧化铝和盐酸的物质的量的比值是1:3,所以氢氧化铝的物质的量是:0.02mol,
故答案为:
n(MgCO3):n(Mg(OH)2):n(Al(OH)3)=1:5:2
分析:(1)根据遇酸及酸性药物则产生二氧化碳,说明含有碳酸根离子或碳酸氢根离子,水溶液呈弱碱性,说明是强碱弱酸盐,灼烧时火焰为黄色,说明含有钠离子,白色结晶状粉末,受热可缓缓分解,碳酸钠不会分解,所以只能是碳酸氢钠;
根据可溶于稀酸或氢氧化钠溶液中,该物质是一种两性碱,凝胶本身覆盖于溃疡面上,具有保护作用,说明该物质遇水会生成胶状物质,所以该物质是氢氧化铝;
(2)根据离子方程式的书写原则进行分析;
(3)根据镁元素、硅元素、和氢元素的化合价以及氧化物的定义进行书写;
根据题中的叙述找出反应物、生成物书写方程式;
(4)根据标准状况下224mL气体,计算出二氧化碳的摩尔数,依据二氧化碳的摩尔数计算出碳酸镁的物质的量,根据Mg(OH)2在高温下分解为MgO,取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4g可知,所以2.4克固体是氧化镁,计算出氧化镁的物质的量,在计算出氯化镁物质的量,就可以得到氢氧化镁物质的量,进而计算消耗盐酸物质的量,通过盐酸物质的量就可以得到氯化铝物质的量.
点评:在解此类题时,首先读懂题意,然后结合学过的知识和题中的知识进行解答,需要注意物质的量的求解.
(1)遇酸及酸性药物则产生二氧化碳,说明含有碳酸根离子或碳酸氢根离子,水溶液呈弱碱性,说明是强碱弱酸盐,灼烧时火焰为黄色,说明含有钠离子,白色结晶状粉末,受热可缓缓分解,碳酸钠不会分解,所以只能是碳酸氢钠;可溶于稀酸或氢氧化钠溶液中,该物质是一种两性碱,凝胶本身覆盖于溃疡面上,具有保护作用,说明该物质遇水会生成胶状物质,所以该物质是氢氧化铝,故答案为:NaHCO3;Al(OH)3;
(2)碳酸氢钠和盐酸的反应实质就是碳酸氢根离子和氢离子会生成水的反应,故答案为:HCO3-+H+═H2O+CO2↑;
(3)镁元素显+2价,硅元素显+4价,氢元素显+1价,氧元素显-2价,氧化物中只有氧和另一种元素,故答案为:2MgO?3SiO2?nH2O;
三硅酸镁和盐酸反应生成氯化镁、硅酸和水,故答案为:Mg2Si3O8?nH2O+4HCl=2MgCl2+3H2SiO3↓+(n-1)H2O;
(4)标准状况下224mL气体的物质的量是:
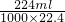 =0.01mol,
=0.01mol,设生成0.01mol的二氧化碳需要碳酸镁物质的量是x,消耗盐酸物质的量是y,生成氯化镁物质的量是z,
MgCO3+2HCl=MgCl2+H2O+CO2↑
1 2 1 1
x y z 0.01
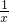 =
= =
= =
=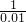
x=0.01mol y=0.02mol z=0.01mol
MgCl2+2NaOH=2NaCl+Mg(OH)2↓ Mg(OH)2
 MgO+H2O
MgO+H2O从方程式中可以看出氧化镁的物质的量和氯化镁的物质的量是相当的,
氧化镁物质的量:
 =0.06mol,所以氯化镁物质的量也是0.06mol;碳酸镁生成0.01mol的氯化镁,所以氢氧化镁生成0.05mol的氯化镁,
=0.06mol,所以氯化镁物质的量也是0.06mol;碳酸镁生成0.01mol的氯化镁,所以氢氧化镁生成0.05mol的氯化镁,设生成0.05mol的氯化镁需要氢氧化镁m,消耗盐酸n,
Mg(OH)2+2HCl=MgCl2+2H2O
1 2 1
m n 0.05mol
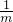 =
=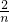 =
=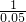
m=0.05mol n=0.1mol
所以与氢氧化铝反应的盐酸物质的量是:
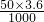 -0.1-0.02=0.06mol,
-0.1-0.02=0.06mol,Al(OH)3+3HCl=AlCl3+3H2O,从方程式中可以看出氢氧化铝和盐酸的物质的量的比值是1:3,所以氢氧化铝的物质的量是:0.02mol,
故答案为:
n(MgCO3):n(Mg(OH)2):n(Al(OH)3)=1:5:2
分析:(1)根据遇酸及酸性药物则产生二氧化碳,说明含有碳酸根离子或碳酸氢根离子,水溶液呈弱碱性,说明是强碱弱酸盐,灼烧时火焰为黄色,说明含有钠离子,白色结晶状粉末,受热可缓缓分解,碳酸钠不会分解,所以只能是碳酸氢钠;
根据可溶于稀酸或氢氧化钠溶液中,该物质是一种两性碱,凝胶本身覆盖于溃疡面上,具有保护作用,说明该物质遇水会生成胶状物质,所以该物质是氢氧化铝;
(2)根据离子方程式的书写原则进行分析;
(3)根据镁元素、硅元素、和氢元素的化合价以及氧化物的定义进行书写;
根据题中的叙述找出反应物、生成物书写方程式;
(4)根据标准状况下224mL气体,计算出二氧化碳的摩尔数,依据二氧化碳的摩尔数计算出碳酸镁的物质的量,根据Mg(OH)2在高温下分解为MgO,取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4g可知,所以2.4克固体是氧化镁,计算出氧化镁的物质的量,在计算出氯化镁物质的量,就可以得到氢氧化镁物质的量,进而计算消耗盐酸物质的量,通过盐酸物质的量就可以得到氯化铝物质的量.
点评:在解此类题时,首先读懂题意,然后结合学过的知识和题中的知识进行解答,需要注意物质的量的求解.

练习册系列答案
相关题目