题目内容
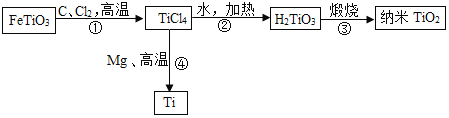
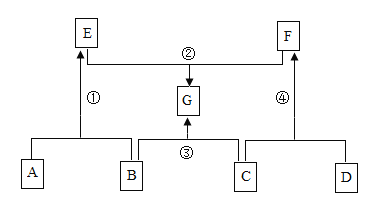
【题目】A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去)。其中A、B、C中均含有同一种元素,D是温室气体,G是重要调味品。G的化学式为__________。反应①的基本反应类型为_______________。反应③的化学方程式为________
【答案】NaCl 复分解反应 NaOH+HCl=NaCl+H2O
【解析】
A、B、C中均含有同一种元素,D是温室气体,则D为二氧化碳;G是重要调味品,则G为氯化钠;二氧化碳和C反应会生成F,所以C是氢氧化钠,F是碳酸钠;B和氢氧化钠会生成氯化钠,所以B是盐酸;碳酸钠和E反应会生成氯化钠,所以E是氯化钙;A和盐酸反应生成氯化钙,所以A是氢氧化钙。
G的化学式为:NaCl。反应①氢氧化钙与稀盐酸反应产生氯化钙和水,符合“两交换、不变价”属于复分解反应。反应③氢氧化钠与稀盐酸发生酸碱中和反应产生氯化钠和水的化学方程式为:NaOH+HCl=NaCl+H2O。

【题目】学习了二氧化锰对过氧化氢有催化作用的知识后。某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行了如下探究。
(猜想)Ⅰ.氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ.氧化铜是反应的催化剂,反应前后_____和_____不变。
(实验)用天平称量0.2g氧化铜,取5mL 5%的过氧化氢溶液于试管中,进行如下实验:
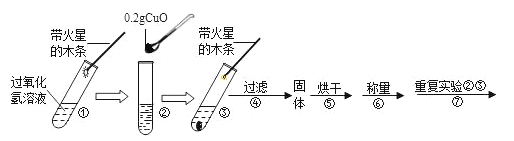
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____, 带火星的木条复燃 | 所得固体 _____g | 溶液中有气泡放出, _____ | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(2)步骤①的目的是_____。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为_____。
【题目】小雨发现一种神奇的蜡烛,点燃后发现怎么也“吹不灭”,于是对这种蜡烛产生了浓厚的兴趣,下面请你和小雨一起进行探究。

[查阅资料]
普通蜡烛由石蜡和烛芯制成,吹不灭的蜡烛在普通蜡烛的烛芯外包裹了一层打火石。打火石是在某种金属中掺入少量稀土元素制成的合金,它的着火点只有150°C蜡烛燃烧时包裹在石蜡内的打火石并不燃烧,当吹“灭”蜡烛时,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
[问题与思考]
(1)蜡烛燃烧时,包裹在石蜡内的打火石并不燃烧,原因是:_____,如果将这种蜡烛熄灭,你应采用的方法是_____。
(2)蜡烛芯外包裹的打火石中的金属是什么?
[实验探究]
吹不灭的蜡烛芯外的打火石含的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,他们决定继续探究。(不考虑打火石中稀土元素对探究金属性质的影响)
实验序号 | 实验操作 | 现象 | 结论 |
1 | 取该打火石,用砂纸打磨后观察 | 打火石呈_____色 | 打火石中的金属一定不是铜 |
2 | 取少量打磨后的打火石于试管中,加入稀盐酸 | 有气泡产生,溶液无色 | 打火石中的金属一定不是_____。 |
3 | 将少量打磨后打火石加入到硫酸铜溶液中 | 打火石表面有红色物质析出 | 打火石中的金属一定是镁 |
[讨论交流]
(1)实验3中涉及的化学方程式为_____。
(2)你认为实验3的方案是否合理_____(填“是”或“否”),如合理请说明理由,如不合理请设计一个方案进一步确认该金属是镁:_____。