题目内容
从化学方程式2KClO3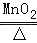 2KCl+3O2↑中获取的信息错误的是( )
2KCl+3O2↑中获取的信息错误的是( )
A.反应生成了气体
B.反应物是KClO3和MnO2,生成物是KCl和O2
C.反应物与生成物的粒子个数比为2:2:3
D.245g KClO3完全反应生成149g KCl和96g O2
 阅读快车系列答案
阅读快车系列答案用不纯的锌片(杂质不参加反应)与稀硫酸反应,六次实验结果记录如下:(计算结果均取整数)
次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加入锌的质量(g) | 2 | 4 | 6 | 8 | 10 | 12 |
稀硫酸的质量(g) | 60 | 60 | 60 | 60 | 60 | 60 |
生成的硫酸锌的质量(g) | 5 |
| 15 | 17 |
| 17 |
(1)将第2次和第5次实验产生的硫酸锌的质量填在上表中;
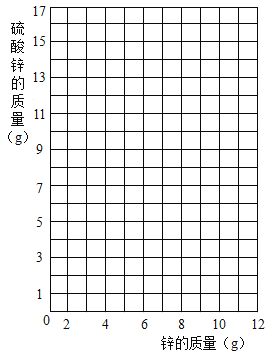
(2)在右图中画出硫酸锌与锌的质量函数关系的曲线;
(3)若将(10+m)g这种锌片放入60g这种稀硫酸中,充分反应后剩余固体的质量为 g;
(4)该实验所使用的稀硫酸中溶质的质量分数为 .
在验证铝和铜的金属活动性强弱时,同学们发现铝与氯化铜溶液反应现象明显,而铝与硫酸铜溶液反应现象不明显。某小组同学进行如下探究:
(提出问题)铝与氯化铜溶液反应较铝与硫酸铜溶液反应现象明显的原因是什么?
(猜想)猜想一:铝表面有氧化膜;猜想二:氯离子对铝置换铜离子的反应有促进作用;猜想三:硫酸根离子对铝置换铜离子的反应有抑制作用。
(设计实验)同学们准备质量相等、大小相同且除去氧化膜的铝片,分别配制了质量、浓度均相等的氯化铜和硫酸铜溶液进行了如下实验:
实验操作 | 实验现象 | 实验结论 |
(1)将两块铝片分别插入氯化铜溶液、硫酸铜溶液中 | 插入氯化铜溶液中的铝片上很快产生大量海绵状红色物质,插入硫酸铜溶液中的铝片现象不明显 | _________ |
(2)取两支试管加入铝片和硫酸铜溶液,向其中一支试管中加入1g氯化钠固体 | _________ | 猜想二正确 |
(3)_________ | _________ | 猜想三不正确 |
(分析)实验操作(2)中氯化钠能否用稀盐酸代替?并说明原因_______________。
(拓展)实验操作(1)中铝片插入氯化铜溶液中有气泡产生,产生的气体可能是氢气或氧气中的一种(假设收集到的气体为纯净气体),请设计实验确定该气体是什么(写出操作方法及预期现象)_________。


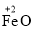 :氧化铁中铁元素的化合价为+2价
:氧化铁中铁元素的化合价为+2价
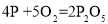
 H2+CO,反应前后,发生了变化的是
H2+CO,反应前后,发生了变化的是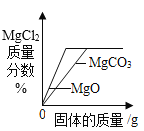 将足量的碳酸镁和氧化镁固体分别加入相同质量、相同溶质质量分数的稀盐酸中
将足量的碳酸镁和氧化镁固体分别加入相同质量、相同溶质质量分数的稀盐酸中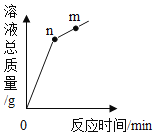 将盐酸逐渐加入氧化铜中,n点和m点对应溶液中铜元素质量相等
将盐酸逐渐加入氧化铜中,n点和m点对应溶液中铜元素质量相等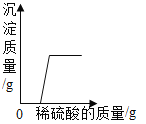 向氢氧化钠和硝酸钡的混合溶液中,逐滴滴加稀硫酸
向氢氧化钠和硝酸钡的混合溶液中,逐滴滴加稀硫酸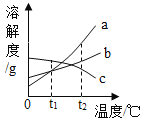 t2℃时等质量的a、b、c三种物质的饱和溶液降温到t1℃,所得溶液中溶剂最少的是a
t2℃时等质量的a、b、c三种物质的饱和溶液降温到t1℃,所得溶液中溶剂最少的是a