题目内容
将锌粒放入硫酸铜溶液,有时有无色无味气体产生的“异常”现象.推测该气体可能是( )
| A、氢气 | B、二氧化硫 | C、二氧化碳 | D、一氧化碳 |
练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
| A、铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 | B、水和过氧化氢的组成元素相同,则两者的化学性质相同 | C、Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 | D、同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率 |
下列实验现象描述完整且正确的是( )
| A、镁条放入稀盐酸中,银白色固体表面会迅速产生大量气泡,放出热量 | B、细铁丝在氧气中燃烧,剧烈燃烧,火星四射,生成黑色固体四氧化三铁,放出大量的热 | C、铝丝浸入硫酸铜溶液后,银白色固体表面有紫红色物质生成,溶液由蓝色逐渐变为无色 | D、在盛有3mL水的试管中,滴入几滴植物油,再滴几滴洗涤剂,振荡,形成的乳浊液不能稳定地存在,液体分为两层 |
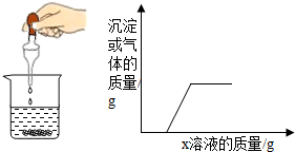 向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入溶液的质量关系符合图乙的是( )
向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入溶液的质量关系符合图乙的是( )| 序号 | 烧杯中的物质 | x溶液 |
| ① | 铜锌合金 | 稀硫酸 |
| ② | 生锈(薄层)的铁钉 | 稀盐酸 |
| ③ | 盐酸和稀硫酸溶液 | 氯化钡溶液 |
| ④ | 氯化钠和碳酸钠溶液 | 稀盐酸 |
| ⑤ | 稀盐酸和硫酸铜溶液 | 烧碱溶液 |
| A、①②③ | B、②⑤ |
| C、②④⑤ | D、③⑤ |
下列图象分别与选项中的操作相对应,其中不合理的是( )
A、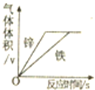 相同的铁、锌分别放入稀盐酸中 | B、 煅烧石灰石(主要成分是CaCO3) | C、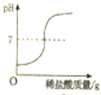 向稀盐酸中不断滴加氢氧化钠溶液 | D、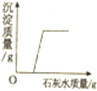 向稀盐酸和氯化铜溶液中加入石灰水 |
向含有Cu(NO3)2和AgNO3 的混合溶液中加入一定量的铁粉,充分反应后,过滤出的金属只有铜和银.则下列对滤液成分的判断不正确的是( )
| A、可能有 AgNO3 | B、一定有 Fe(NO3)2 | C、可能有 Cu(NO3)2 | D、一定无 AgNO3 |
某工厂排放的废液中含有少量硫酸和硫酸铜.取适量废液放入盛有铁粉的烧杯中,搅拌,待充分反应后过滤,得少量滤渣和滤液.关于该实验,下列说法正确的是( )
| A、滤液的酸性比废液的酸性弱 | B、滤液可直接排放 | C、滤渣中一定含铜和铁 | D、滤液的主要成分是硫酸铁 |
FeCl3溶液腐蚀铜、铁的反应分别为:Cu+2FeCl3=2FeCl2+CuCl2、Fe+2FeCl3=3FeCl2.
从腐蚀过镀铜器件的废液中回收铜,并重新制得FeCl3的流程如下:
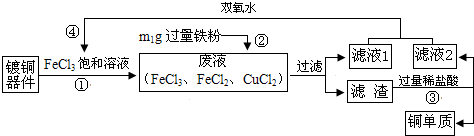
下列说法不正确的是( )
从腐蚀过镀铜器件的废液中回收铜,并重新制得FeCl3的流程如下:

下列说法不正确的是( )
| A、步骤②中发生化合反应与置换反应 | B、“滤液1”中一定含FeCl2,可能含CuCl2 | C、步骤④反应为:2M+2FeCl2+H2O2=2FeCl3+2H2O,M是HCl | D、若滤渣也为m1g,则废液中FeCl3与CuCl2的质量比为65:54 |
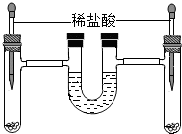 如图,将等质量的锌和铁分别入入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
如图,将等质量的锌和铁分别入入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )| A、右试管中溶液为浅绿色 | B、两试管中所得溶液的质量相等 | C、U型管中液面左升右降 | D、U型管中液面仍相平 |
