��Ŀ����
����Ŀ���кͷ�Ӧ����ȣ����õι���ȡĩ֪Ũ�ȵ�������Һ����μ���ʢ��40g������������Ϊ20%����������Һ���ձ��У�ͬʱ��pH�Ƽ�¼��ҺpH�ı仯�����Ƴ����º���ͼ��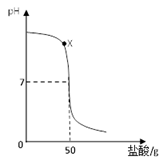
��1���ò�����պȡX����Һ���ھƾ��ƻ����ϼ��������ɣ������������µĹ�����һ�����������ѧʽ��
��2����֤���кͷ�Ӧ����ȡ�����ʹ���������ƹ����ϡ���ᷴӦ������Ϊ
��3���Ը��ݺ���ͼ����������Һ�����ʵ�������������д��������̣�
���𰸡�
��1��NaCl��NaOH
��2��NaOH��������ˮҲ�����,��֤�����кͷ���
��3���⣺������NaCl������Ϊx
NaOH + HCl = | NaCl + H2O |
40 | 58.5 |
40g��20% | x |
![]()
x=7.3g����Һ�����ʵ���������= ![]() ��100%=14.6%��
��100%=14.6%��
����������1������Һ����X��ʱ��pH����7��˵���������ƹ��������Դ�ʱ��Һ�е�������NaCl ��NaOH�������ò�����պȡX����Һ���ھƾ��ƻ����ϼ��������ɣ������������µĹ�����һ�����У�NaCl��NaOH����2����Ϊ�������ƹ�������ˮʱҲ�������������������˵�������������кͷ�Ӧ�ˣ����Բ������������ƹ����ϡ���ᷴӦ��֤���кͷ�Ӧ����ȡ�����3����ͼ�п�֪����pH=7ʱ����ʾ��Ӧǡ����ȫ�����ݷ�Ӧ��NaOH+HCl=NaCl+H2O��NaOH��HCl��������ϵ�����������HCl��������
�����㾫�������ڱ��⿼����кͷ�Ӧ����Ӧ�ú��ݻ�ѧ��Ӧ����ʽ�ļ��㣬��Ҫ�˽��кͷ�Ӧ����������������κ�ˮ�ķ�Ӧ�������ʼ�������=ϵ������Է�������֮�Ȳ��ܵó���ȷ�𰸣�

����Ŀ����ȥ�����е��������ʣ�����ʵ�鷽�����ܴﵽʵ��Ŀ�ĵ��ǣ�������
ʵ��Ŀ�� | ʵ�鷽�� | |
A | ��ȥͭ���л��е��������� | ��������������� |
B | ��ȥFeCl2Һ�е�����CuCl2 | ������������ۣ����� |
C | ��ȥN2�е�O2 | ����ͨ������ͭ˿�� |
D | ��ȥCO�л��е�����CO2 | ������ͨ�������ȵ�����ͭ |
A.AB.BC.CD.D
