题目内容
7 分)(1)锌片长期暴露在空气中表面会形成一层薄膜,其主要成分是碱式碳酸锌【Zn2(OH)2CO3】。若该物质通过化合反应生成,反应物除 Zn 外,还有 ①N2 ②O2 ③CO2 ④H2O中的( )
| A.一种 | B.两种 | C.三种 | D.四种 |
①反应中产生的气体的质量是 g。
②计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数)。
③如果铁钉的铁锈未除净,对硫酸的质量分数的计算结果的影响是“偏大”“偏小”、 无影响”),理由是 。
(1)C(1分) (2)①0.1(1分)②32.7%;③偏小(1 分);硫酸与铁锈反应(1 分)
解析试题分析:(1)根据质量守恒定律反应前后原子的种类和数量不变,可知还要有,二氧化碳、水、氧气;
(2)根据质量守恒定律知:33.2g+10.8g-43.9g=0.1g
②解:硫酸废液的质量为33.2g—18.2g=15g(0.5分)
设样品中H2SO4的质量为x
Fe+ H2SO4=FeSO4+ H2↑(1分)
98 2
x 0.1g
x=4.9g(0.5分)
硫酸的质量分数为:4.9g/15g×100%≈32.7%(1分)
考点:质量守恒定律,根据化学方程式的计算

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
化学用语既能描述宏观物质,也能表达其微观的变化。
(1)下列符号能表示2个氢原子的是 (填写序号,下同),能表示保持水的化学性质的微粒是 。
| A.H2 | B.2H | C.H2O | D.2H2O |
(3)看图回答问题:
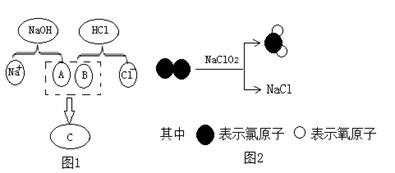
①图1描述了NaOH溶液与盐酸反应的微观实质,图中C处应填入的化学式为 。
②图2表示反应的化学方程式为 。