题目内容
【题目】下表为元素周期表中某一周期元素的原子结构示意图.请回答下列问题: 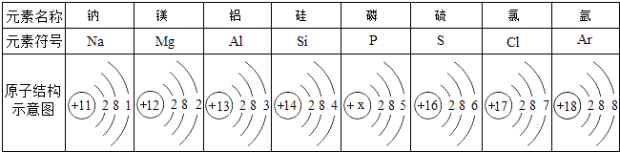
(1)表中磷原子的核电荷数x=;决定原子的种类;
(2)表中具有相对稳定结构的元素是;
(3)镁元素与氯元素形成的化合物化学式为;
(4)上述元素在周期表中处于同一周期的原因是;
(5)原子的化学性质与有关.
【答案】
(1)15;质子数(即核电荷数)
(2)氩
(3)MgCl2
(4)原子核外电子层数相同
(5)原子的最外层电子数
【解析】解:(1)原子中质子数=核外电子数,则磷原子的核电荷数x=2+8+5=15.
元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),(2)氩元素的最外层为电子数均为8,均属于相对稳定结构.(3)镁原子的最外层电子数为2,在化学反应中易失去2个电子而形成带2个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+2价;氯原子的最外层电子数为7,在化学反应中易得到1个电子而形成1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为﹣1价;镁元素显+2价,氯元素显﹣1价,镁和氯组成化合物的化学式为MgCl2 . (4)由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.(5)元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是原子的最外层电子数.
故答案为:(1)15;质子数(即核电荷数);(2)氩;(3)MgCl2;(4)原子核外电子层数相同;(5)原子的最外层电子数.
(1)根据原子中质子数=核外电子数,结合元素的概念,进行分析解答.(2)若粒子的最外层电子数为8(氦为2个),属于相对稳定结构.(3)化合价的数值等于离子所带电荷的数值,且符号一致,由镁、氯元素的最外层电子数确定元素的化合价,进行分析解答.(4)根据元素周期数与电子层数的关系,进行分析解答.(5)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析解答.

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g氧化铜均匀混合加热
Ⅱ中x的值应为 ;在相同温度下,比较两组实验收集相同体积的氧气所需要的
②乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
本实验中,测量O2体积的装置是 (填编号).
实验结论:在相同条件下, ,双氧水分解得越快.