题目内容
(2011年山东德州,2题)小明同学想测量某赤铁矿样品中氧化铁的纯度(假设其他成分不和酸反应,也不溶于水),进行如下实验:称取10g赤铁矿样品,加入到烧杯中,再加入92.5g的稀硫酸,恰好完全反应。过滤得滤渣2.5g。试计算:
(1)赤铁矿样品中氧化铁的质量分数?
解:(1)赤铁矿样品中氧化铁的质量分数为: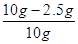 ×100% =" 75%"
×100% =" 75%"
(2)设反应所得滤液中硫酸铁的质量为x
Fe2O3 + 3H2SO4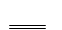 Fe2(SO4)3 + 3H2O
Fe2(SO4)3 + 3H2O
160 400
7.5g x
160:400="7.5g:" x x=" 18.75g"
反应所得滤液中溶质的质量分数为: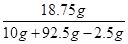 ×100%="18.75%"
×100%="18.75%"
答:(略)
解析

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目



