题目内容
【题目】把一定质量的纯净物 E 和 40 克的纯净物 F 按如图的微观过程进行反应。反应结束后,可生成 44 克 G物质和 9 克 H 物质。关于该反应的说法正确的是
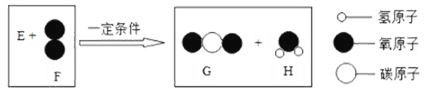
A. 9 克 H 物质中氢元素的质量为 2 克
B. G 和 H 的分子个数比为 1:2
C. E 为含氧化合物
D. E 分子中原子个数比为 1:1
【答案】D
【解析】A、H分子为1个氧原子和2个氢原子构成的水分子,则9g水中氢元素的质量=9g×![]() ×100%=1g,即9g物质H中含氢元素质量为1g,故A错误;
×100%=1g,即9g物质H中含氢元素质量为1g,故A错误;
B、根据反应生成物G、H的分子构成可判断两种生成物中共含C、H、O三种元素,而反应物F中只含O元素,根据化学变化前后元素种类不变,可判断反应E中一定含C、H两种元素,不能确定物质E中是否含O元素;再由生成44g)G物质和9g H物质中含O的总质量=44g×![]() +9g×
+9g×![]() =40g,若40g氧气完全反应,E不含氧元素,故B不正确;C、由微观图,可判断G为CO2、H为H2O,根据生成G物质44g、H物质9g,结合两物质的相对分子质量,可计算得出反应中物质G与H的分子个数比=44g44:9g18=2:1;故C不正确;D、根据示意图可以看出,E中原子个数比应该为1:1,故D正确;故选:D。
=40g,若40g氧气完全反应,E不含氧元素,故B不正确;C、由微观图,可判断G为CO2、H为H2O,根据生成G物质44g、H物质9g,结合两物质的相对分子质量,可计算得出反应中物质G与H的分子个数比=44g44:9g18=2:1;故C不正确;D、根据示意图可以看出,E中原子个数比应该为1:1,故D正确;故选:D。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目