题目内容
(2012?武清区二模)实验室用6.5g锌与足量稀盐酸反应,可制得氢气多少克?这些氢气在标准状况下为多少升?(氢气的密度是0.09g/L)计算结果保留至0.01.
分析:首先应根据反应物、生成物、反应条件正确的写出化学方程式,然后根据方程式找出锌与氢气的质量关系,从而求出制得氢气的质量,再根据公式:体积═
求出这些氢气的体积
| 质量 |
| 密度 |
解答:解:设生成氢气的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
6.5g x
=
x=0.2g
氢气在标准状况下的体积为
=2.22l
答:生成氢气0.2g,在标准状况下2.22升
Zn+2HCl═ZnCl2+H2↑
65 2
6.5g x
| 65 |
| 6.5g |
| 2 |
| x |
x=0.2g
氢气在标准状况下的体积为
| 0.2g |
| 0.09g/L |
答:生成氢气0.2g,在标准状况下2.22升
点评:本题是一道联系密度公式的综合学科题,考查了同学们用化学知识分析解决问题的能力.

练习册系列答案
相关题目

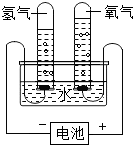 (2012?武清区二模)通过分析实验结果推断物质的组成,是认识物质的一种方法.研究水的组成就是利用了这种方法.电解水实验结果如图所示.
(2012?武清区二模)通过分析实验结果推断物质的组成,是认识物质的一种方法.研究水的组成就是利用了这种方法.电解水实验结果如图所示.