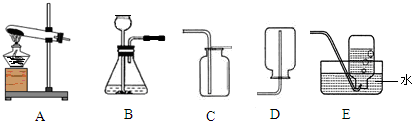题目内容
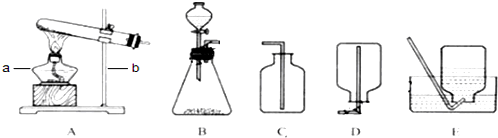
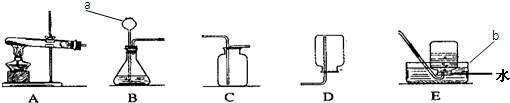
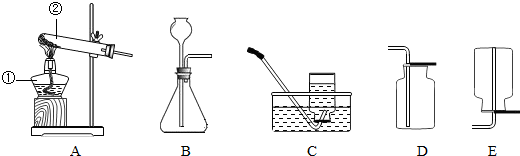
请根据下列实验装置图回答问题.
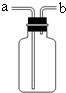
(1)写出仪器a、b的名称,a是______,b是______.
(2)若用B装置制取二氧化碳,反应的化学方程式是______.稀盐酸一滴入锥形瓶内立即用排水法收集一集气瓶二氧化碳做蜡烛熄灭实验,蜡烛没有熄灭的原因是______.
(3)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.该反应的化学方程式是______ CaCl2+2NH3↑+2H2O
【答案】分析:(1)熟悉常见仪器,了解名称;
(2)根据B装置适用于固体和液体的不加热反应分析解题;
(3)根据信息:实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.写出化学方程式,并据装置选取方法选择实验装置;
(4)收集氨气时应选用D装置,说明氨气的密度小于空气的密度;集气瓶内有大量红色液体进入,说明氨气极易溶于水形成氨水.
解答:解:(1)图中a是试管,b是分液漏斗;
(2)B装置适用于固体和液体的不加热反应,制取二氧化碳可用大理石和稀盐酸反应生成二氧化碳的同时,还生成氯化钙和水,化学反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;稀盐酸一滴入锥形瓶内立即用排水法收集,此时出来的气体中多数是空气,故蜡烛没有熄灭;
(3)用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水,方程式是:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O;制得氨气是用加热氯化铵和氢氧化钙固体混合物的方法,属于“固体加热型”,所以选择A;
CaCl2+2NH3↑+2H2O;制得氨气是用加热氯化铵和氢氧化钙固体混合物的方法,属于“固体加热型”,所以选择A;
(4)收集氨气时应选用D装置,说明氨气的密度小于空气的密度;氨水显碱性,碱性溶液可使酚酞试液变红,集气瓶内有大量红色液体进入,说明氨气极易溶于水形成氨水;
故答案为:(1)试管; 分液漏斗;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑; 集气瓶内混有大量空气,应待导管口冒出的气泡均匀、稳定时才可收集;
(3)2NH4Cl+Ca(OH)2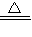 CaCl2+2NH3↑+2H2O; A;
CaCl2+2NH3↑+2H2O; A;
(4)易溶于水;密度比空气小等.
点评:本题主要考查仪器的名称、装置的选取、方程式的书写等知识,考查全面,要依据相关知识细心分析.
(2)根据B装置适用于固体和液体的不加热反应分析解题;
(3)根据信息:实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.写出化学方程式,并据装置选取方法选择实验装置;
(4)收集氨气时应选用D装置,说明氨气的密度小于空气的密度;集气瓶内有大量红色液体进入,说明氨气极易溶于水形成氨水.
解答:解:(1)图中a是试管,b是分液漏斗;
(2)B装置适用于固体和液体的不加热反应,制取二氧化碳可用大理石和稀盐酸反应生成二氧化碳的同时,还生成氯化钙和水,化学反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;稀盐酸一滴入锥形瓶内立即用排水法收集,此时出来的气体中多数是空气,故蜡烛没有熄灭;
(3)用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水,方程式是:2NH4Cl+Ca(OH)2
 CaCl2+2NH3↑+2H2O;制得氨气是用加热氯化铵和氢氧化钙固体混合物的方法,属于“固体加热型”,所以选择A;
CaCl2+2NH3↑+2H2O;制得氨气是用加热氯化铵和氢氧化钙固体混合物的方法,属于“固体加热型”,所以选择A;(4)收集氨气时应选用D装置,说明氨气的密度小于空气的密度;氨水显碱性,碱性溶液可使酚酞试液变红,集气瓶内有大量红色液体进入,说明氨气极易溶于水形成氨水;
故答案为:(1)试管; 分液漏斗;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑; 集气瓶内混有大量空气,应待导管口冒出的气泡均匀、稳定时才可收集;
(3)2NH4Cl+Ca(OH)2
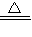 CaCl2+2NH3↑+2H2O; A;
CaCl2+2NH3↑+2H2O; A;(4)易溶于水;密度比空气小等.
点评:本题主要考查仪器的名称、装置的选取、方程式的书写等知识,考查全面,要依据相关知识细心分析.

练习册系列答案
相关题目