题目内容
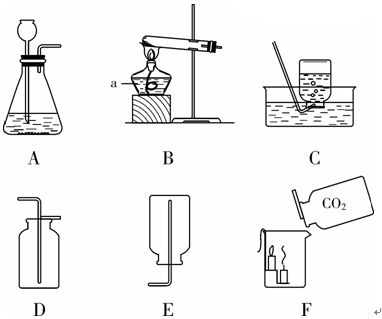
下图所示的实验装置我们常用:

⑴ 实验室制取氧气的一个化学方程式是 ① 。根据该反应原理我选用制取氧气的发生装置是 ② (填装置字母代号,下同),收集装置是 ③ 。
⑵ 检查装置B气密性的方法是 ④ 。
⑶用这些装置还可以进行实验探究。例如:碳酸氢铵(NH4HCO3)是一种常见的固态氮肥。碳酸氢铵受热易分解产生三种化合物,其中一种是氨气(NH3)。我猜想另外两种生成物是 ⑤ ;为了证明我的猜想,将A中生成的物质依次通过G装置和F装置,观察到G中现象 ⑥ ,F中现象是 ⑦ 。

⑴ 实验室制取氧气的一个化学方程式是 ① 。根据该反应原理我选用制取氧气的发生装置是 ② (填装置字母代号,下同),收集装置是 ③ 。
⑵ 检查装置B气密性的方法是 ④ 。
⑶用这些装置还可以进行实验探究。例如:碳酸氢铵(NH4HCO3)是一种常见的固态氮肥。碳酸氢铵受热易分解产生三种化合物,其中一种是氨气(NH3)。我猜想另外两种生成物是 ⑤ ;为了证明我的猜想,将A中生成的物质依次通过G装置和F装置,观察到G中现象 ⑥ ,F中现象是 ⑦ 。
略
分析:(1)根据实验室制氧气的原理和氧气的性质回答.
(2)根据利用气压原理检查装置的气密性.
(3)根据质量守恒定律、碳酸氢盐的性质及水和二氧化碳的检验方法回答.
解答:解:
(1)实验室制氧气的原理有三种:一是过氧化氢催化分解,二是加热分解高锰酸钾,三是在加热和催化剂条件下,分解氯酸钾,方程式分别是:2H2O2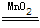 2H2O+O2↑、2KMnO4
2H2O+O2↑、2KMnO4 K2MnO4+MnO2+O2↑、2KClO3
K2MnO4+MnO2+O2↑、2KClO3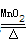 2KCl+3O2↑;如用过氧化氢制氧气,选择装置B,如用加热氯酸钾的方法制氧气,选择装置A;由于氧气不易溶解于水,可用排水法收集,由于氧气的密度比空气大,可用向上排空气法收集.
2KCl+3O2↑;如用过氧化氢制氧气,选择装置B,如用加热氯酸钾的方法制氧气,选择装置A;由于氧气不易溶解于水,可用排水法收集,由于氧气的密度比空气大,可用向上排空气法收集.
(2)可利用气压变化原理检查装置的气密性,先用止水夹夹紧导管b,向长颈漏斗中注入水至浸没长颈漏斗下端,继续加水,液面不下降.
(3)碳酸氢盐受热易分解生成碳酸盐、水、二氧化碳,可推知:碳酸氢铵受热分解生成碳酸铵、水、二氧化碳;如产物中有水,则可观察到G中固体由无色变成蓝色;如产物中有二氧化碳,则F中澄清的石灰水变浑浊.
故答案为:
(1)2H2O2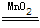 2H2O+O2↑(或2KClO3
2H2O+O2↑(或2KClO3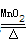 2KCl+3O2↑);B(或A);C或E.
2KCl+3O2↑);B(或A);C或E.
(2)用止水夹夹紧导管b,向长颈漏斗中注入水至浸没长颈漏斗下端,继续加水,液面不下降.
(3)水、二氧化碳;固体由无色变成蓝色;澄清的石灰水变浑浊.
(2)根据利用气压原理检查装置的气密性.
(3)根据质量守恒定律、碳酸氢盐的性质及水和二氧化碳的检验方法回答.
解答:解:
(1)实验室制氧气的原理有三种:一是过氧化氢催化分解,二是加热分解高锰酸钾,三是在加热和催化剂条件下,分解氯酸钾,方程式分别是:2H2O2
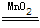 2H2O+O2↑、2KMnO4
2H2O+O2↑、2KMnO4 K2MnO4+MnO2+O2↑、2KClO3
K2MnO4+MnO2+O2↑、2KClO3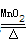 2KCl+3O2↑;如用过氧化氢制氧气,选择装置B,如用加热氯酸钾的方法制氧气,选择装置A;由于氧气不易溶解于水,可用排水法收集,由于氧气的密度比空气大,可用向上排空气法收集.
2KCl+3O2↑;如用过氧化氢制氧气,选择装置B,如用加热氯酸钾的方法制氧气,选择装置A;由于氧气不易溶解于水,可用排水法收集,由于氧气的密度比空气大,可用向上排空气法收集.(2)可利用气压变化原理检查装置的气密性,先用止水夹夹紧导管b,向长颈漏斗中注入水至浸没长颈漏斗下端,继续加水,液面不下降.
(3)碳酸氢盐受热易分解生成碳酸盐、水、二氧化碳,可推知:碳酸氢铵受热分解生成碳酸铵、水、二氧化碳;如产物中有水,则可观察到G中固体由无色变成蓝色;如产物中有二氧化碳,则F中澄清的石灰水变浑浊.
故答案为:
(1)2H2O2
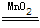 2H2O+O2↑(或2KClO3
2H2O+O2↑(或2KClO3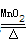 2KCl+3O2↑);B(或A);C或E.
2KCl+3O2↑);B(或A);C或E.(2)用止水夹夹紧导管b,向长颈漏斗中注入水至浸没长颈漏斗下端,继续加水,液面不下降.
(3)水、二氧化碳;固体由无色变成蓝色;澄清的石灰水变浑浊.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目