题目内容
【题目】请用所学化学知识解释下列原理.
(1)刘莹同学在做硫在盛有氧气的集气瓶中燃烧实验时,为了保护空气,在瓶底预先倒入少量的氢氧化钠溶液,其原理为:(写方程式)
(2)现在流行野外露营生活,在野外也要有清洁水源,人们日常生活用水必须经过一系列的净化处理才能使用.向水样中加入明矾,经溶解、(填操作名称),除去不溶性杂质,然后加入活性炭,利用其吸附性除去异味,再杀菌消毒,得到生活用水.欲判断得到的生活用水是硬水还是软水,可用肥皂水检验,其检验方法为
(3)盐酸既是化工的重要产品,又是生产硅材料的重要原料.如图归纳出了盐酸与其他物质间相互反应的关系(图中“﹣”表示相连的两种物质能发生反应),若X是与其他三种不同类别的化合物,则X可以是或(填化学式),根据如图所示物质间关系,写出反应的化学方程式 . 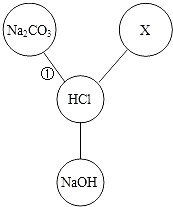
【答案】
(1)SO2+2NaOH=Na2SO3+H2O
(2)过滤,向水中加入肥皂水,泡沫少者为硬水,泡沫多者为软水
(3)Fe2O3(或CuO),Na2CO3+2HCl=2NaCl+H2O+CO2↑
【解析】解:(1)二氧化硫与氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O;(2)为除去水中不溶性固体颗粒,加入明矾使悬浮小颗粒凝聚,经过静置沉降后进行过滤;利用水中钙、镁离子会影响肥皂水的起泡,向水中加入肥皂水,泡沫少者为硬水,泡沫多者为软水;(3)因为我们学过酸的化学性质,酸能与碱反应,酸能与盐反应,酸能与碱性氧化物反应,又因为氢氧化钠属于碱,碳酸钠属于盐,就少了碱性氧化物反应这种类型,所以我们可以选择学过的最常见的碱性氧化物氧化铁、氧化铜等.
根据复分解反应发生的实质,碳酸钠与盐酸反应生成氯化钠、二氧化碳和水方程式是:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
所以答案是:(1)SO2+2NaOH=Na2SO3+H2O(2)过滤;向水中加入肥皂水,泡沫少者为硬水,泡沫多者为软水;(3)4Cl2+CH4 ![]() CCl4+4HCl;(4)Fe2O3(或CuO);Na2CO3+2HCl=2NaCl+H2O+CO2↑.
CCl4+4HCl;(4)Fe2O3(或CuO);Na2CO3+2HCl=2NaCl+H2O+CO2↑.
【考点精析】通过灵活运用氧气的化学性质和水的净化,掌握氧气的化学性质:特有的性质:支持燃烧,供给呼吸;水的净化效果由低到高的是静置、吸附、过滤、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭即可以解答此题.