题目内容
【题目】在学校的元旦联欢会上,小明表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。这是什么原因呢?请你和小明同学进行实验探究。
[提出问题] 过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想] ①可能有一种气体和另一种物质生成;②反应过程中可能有能量变化。
[实验探究] 设计了如右图所示的装置进行探究。
实验一:探究反应后生成的气体是什么?
(1)打开下图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是_______。
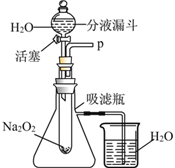
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因是:____________________。
实验二:探究反应后生成的另一种物质是什么?
小红猜想另一种物质可能是Na2CO3,请你写出碳酸钠与盐酸反应的化学方程式:____________________________________。
为了证实小红的猜想,请你设计一个实验:证明生成物中没有Na2CO3:
实验操作 | 实验现象 | 实验结论 |
_______________ | _______________ | ______________ |
小明认为不做上述实验也可以从理论上说明小红的猜想是错误的,请你说出小明的理由:________________________________。
【答案】 氧气 反应放热,使锥形瓶中空气膨胀,从而有气泡冒出 Na2CO3+2HCl === 2NaCl+H2O+CO2↑ ①取少量生成物于试管;②加入少量稀盐酸,立即塞上带管橡皮塞;③将长直导管插入澄清石灰水中 无气体产生,石灰水不变浑浊 不含碳酸钠 根据质量守恒定律,反应前没有碳元素,反应后不可能产生含碳元素的物质
【解析】能使带火星的木条复燃的物质是氧气;
导管口有气泡冒出,说明锥形瓶中的气体受热膨胀,从而说明该反应放出热量; 碳酸钠与盐酸反应生成氯化钠、二氧化碳、和水,反应的方程式为:Na2CO3+2HCl ==2NaCl+H2O+CO2↑;根据二氧化碳能与盐酸反应生成二氧化碳,生成的二氧化碳又能使澄清石灰水变浑浊,故实验步骤为①取少量生成物于试管;②加入少量稀盐酸,立即塞上带管橡皮塞;③将长直导管插入澄清石灰水中;如果没有气体生成,澄清石灰水也不变浑浊,则说明生成物中没有碳酸钠;根据质量守恒定律可知,反应物中不含有碳元素,故生成物中不可能有含碳元素的碳酸钠生成;

【题目】物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成丙。甲、乙、丙的微观示意图见下表。请完成下列空白。
物质 | 甲 | 乙 | 丙 |
|
微观示意图 |
|
|
|
(1)甲、乙、丙3种物质都是由(填“分子”“原子”或“离子”) _______构成的。
(2)甲、乙、丙中属于化合物的是_______。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为_______。
(4)丙中氮、氢元素的质量比为_______。
(5)写出甲和乙在高温、高压、催化剂的条件下合成丙的化学方程式:______________。
