题目内容
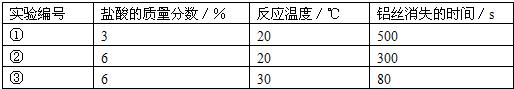
小明选择“铝丝和盐酸反应的快慢与什么因素有关”的课题开展探究,下表是他分别用相同质量的铝丝和足量的稀盐酸反应的三组实验数据:
(1)写出铝和盐酸反应的化学方程式:
(2)实验②和③标明该反应快慢与
(3)能标明盐酸质量分数对反应快慢有影响的实验编号是
| 序号 | 盐酸的质量分数/% | 反应温度/℃ | 铝丝消失的时间/s |
| ① | 3 | 20 | 500 |
| ② | 6 | 20 | 300 |
| ③ | 6 | 30 | 80 |
2Al+6HCl=2AlCl3+3H2↑
2Al+6HCl=2AlCl3+3H2↑
.(2)实验②和③标明该反应快慢与
温度
温度
有关.(3)能标明盐酸质量分数对反应快慢有影响的实验编号是
①
①
和②
②
.分析:(1)熟练掌握铝与盐酸的反应;
(2)比较②和③可以看出它们的不同之处是在于温度;
(3)①和②中两者温度相同的条件下,只是质量分数的差异,故能表明盐酸浓度对反应影响的是①和②.
(2)比较②和③可以看出它们的不同之处是在于温度;
(3)①和②中两者温度相同的条件下,只是质量分数的差异,故能表明盐酸浓度对反应影响的是①和②.
解答:解:(1)铝与盐酸反应是置换反应,要生成氢气和氯化铝,反应的化学方程式:2Al+6HCl=2AlCl3+3H2↑;
(2)②中盐酸质量分数为6%温度为20℃,③中盐酸质量分数为6%温度为30℃,可以看出③所需时间较短,从而可以判断温度不同所需时间也不同;
(3))①和②中两者温度相同的条件下,只是质量分数的差异,故①和②中的数据可知质量分数越大反应所需时间越短.
故答案为:(1)2Al+6HCl=2AlCl3+3H2↑;(2)温度;(3)①;②.
(2)②中盐酸质量分数为6%温度为20℃,③中盐酸质量分数为6%温度为30℃,可以看出③所需时间较短,从而可以判断温度不同所需时间也不同;
(3))①和②中两者温度相同的条件下,只是质量分数的差异,故①和②中的数据可知质量分数越大反应所需时间越短.
故答案为:(1)2Al+6HCl=2AlCl3+3H2↑;(2)温度;(3)①;②.
点评:本题是通过控制不同的量来探究能够影响反应速度的因素的,这类似于物理上所学的控制变量法来解决问题,我们在解答时要注意仔细分析比较,从而得出正确的解答.

练习册系列答案
相关题目