题目内容
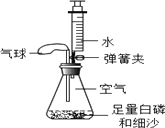
【题目】结合如图所示实验装置,回答下列问题。
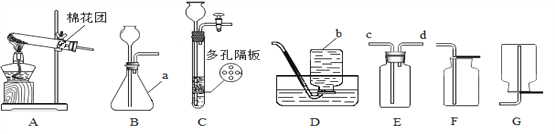
(1)图中a、b仪器的名称:a________,b_______。
(2)用A、D装置制取氧气,反应的化学方程式为___________________________;用排水法收集气体时,当观察到__________时,判断集气瓶中气体已收集满。
(3)若用B装置制取氧气,反应的化学方程式为_______________;所加的液体必须至________;
(4)实验室用装置C制取二氧化碳,与装置B相比,其优点为_______________;如用E装置收集CO2, 验满的方法是_____________________。
(5)Na、Mg等活泼金属可以在CO2中燃烧。某同学收集到一瓶CO2后,通过实验验证Mg条能够在CO2中燃烧。下列物品中他需要使用的有______ (填序号 )
①酒精灯 ②铁架台 ③坩埚钳 ④砂纸 ⑤试管夹
(6)某同学往集气瓶装入半瓶水,再用排水法收集1/2集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃。此集气瓶内的氧气约占总体积的_______%(空气中氧气的体积分数约为21%)。
【答案】 锥形瓶 集气瓶 略 气泡从瓶口向外冒 略 形成液封 控制反应的发生和停止 将燃着的木条放在d导管口 ①③④ 60.5
【解析】(1)图中a、b仪器的名称:a:锥形瓶,b:集气瓶;(2)高锰酸钾法制氧气用A、D装置制取氧气,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;用排水法收集气体时,当观察到集气瓶口有大气泡冒出时,说明集气瓶中气体已收集满;(3)过氧化氢法制氧气时用用B装置制取氧气,反应的化学方程式为2H2O2
K2MnO4+MnO2+O2↑;用排水法收集气体时,当观察到集气瓶口有大气泡冒出时,说明集气瓶中气体已收集满;(3)过氧化氢法制氧气时用用B装置制取氧气,反应的化学方程式为2H2O2![]() 2H2O+O2↑;所加的液体必须至将漏斗末端浸没在液面以下,防止气体从漏斗口逸出;(4)实验室用装置C制取二氧化碳,与装置B相比,其优点为控制反应的发生和停止:关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。;如用E装置收集CO2, 验满的方法是将燃着的木条放在d导管口,木条熄灭,证明已经集满二氧化碳;(5)Na、Mg等活泼金属可以在CO2中燃烧。应用砂纸打磨金属表面的氧化物,用坩埚钳夹取镁条在酒精灯上燃烧; (6) 设集气瓶的容积为100ml,往集气瓶装入半瓶水,则空气为50ml其中氧气为50ml×21%=10.5ml;再用排水法收集1/2集气瓶的氧气,此集气瓶内的氧气约总体积为10.5ml+50ml=60.5ml,其中氧气的含量为60.5ml ÷100ml×100%=60.5%。
2H2O+O2↑;所加的液体必须至将漏斗末端浸没在液面以下,防止气体从漏斗口逸出;(4)实验室用装置C制取二氧化碳,与装置B相比,其优点为控制反应的发生和停止:关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。;如用E装置收集CO2, 验满的方法是将燃着的木条放在d导管口,木条熄灭,证明已经集满二氧化碳;(5)Na、Mg等活泼金属可以在CO2中燃烧。应用砂纸打磨金属表面的氧化物,用坩埚钳夹取镁条在酒精灯上燃烧; (6) 设集气瓶的容积为100ml,往集气瓶装入半瓶水,则空气为50ml其中氧气为50ml×21%=10.5ml;再用排水法收集1/2集气瓶的氧气,此集气瓶内的氧气约总体积为10.5ml+50ml=60.5ml,其中氧气的含量为60.5ml ÷100ml×100%=60.5%。

 阅读快车系列答案
阅读快车系列答案