题目内容
(2013?呼和浩特模拟)某同学取四份50克的水,分别加入一定质量的KNO3固体配制成t℃时的溶液,充分搅拌后过滤去未溶解的固体,将相关数据记录如下:| 操作序号 | 1 | 2 | 3 | 4 |
| 加入KNO3质量/g | 40 | 50 | 60 | 70 |
| 溶液质量/g | 90 | 10 | 105 | 105 |
(2)根据以上数据,计算t℃时KNO3的饱和溶液中溶质质量分数.
【答案】分析:(1)不能再继续溶解硝酸钾的溶液则为饱和溶液,据此分析表中数据,判断达到饱和溶液的实验步骤;
(2)根据记录数据分析饱和溶液中溶质质量,计算此时溶液的溶质质量分数.
解答:解:(1)由记录数据,加入40g硝酸钾溶液质量90g,说明硝酸钾全部溶解;加入50g硝酸钾溶液质量100g,硝酸钾全部溶解;加入60g硝酸钾溶液质量105g,说明此时硝酸钾未溶解完,溶液已饱和;
故答案为:3;
(2)溶液饱和时,50g水中溶解硝酸钾质量=105g-50g=55g,溶液的溶质质量分数=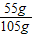 ×100%=52.4%
×100%=52.4%
故答案:t℃时KNO3的饱和溶液中溶质质量分数为52.4%.
点评:利用溶液质量=溶质质量+溶剂质量分析记录数据,可判断每次实验中溶质的溶解情况.
(2)根据记录数据分析饱和溶液中溶质质量,计算此时溶液的溶质质量分数.
解答:解:(1)由记录数据,加入40g硝酸钾溶液质量90g,说明硝酸钾全部溶解;加入50g硝酸钾溶液质量100g,硝酸钾全部溶解;加入60g硝酸钾溶液质量105g,说明此时硝酸钾未溶解完,溶液已饱和;
故答案为:3;
(2)溶液饱和时,50g水中溶解硝酸钾质量=105g-50g=55g,溶液的溶质质量分数=
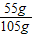 ×100%=52.4%
×100%=52.4%故答案:t℃时KNO3的饱和溶液中溶质质量分数为52.4%.
点评:利用溶液质量=溶质质量+溶剂质量分析记录数据,可判断每次实验中溶质的溶解情况.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目