题目内容
2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)食盐中常添加碘酸钾(KIO3)以补充碘元素.其中碘元素的化合价为
(2)碘酸钾(KIO3)中K、I、O 三种元素的质量比为
(3)服用碘片治疗131I辐射的推荐服用剂量是每日摄入KI为130-170mg,假设服用某碘片每日补充166mg KI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
(1)食盐中常添加碘酸钾(KIO3)以补充碘元素.其中碘元素的化合价为
+5价
+5价
.(2)碘酸钾(KIO3)中K、I、O 三种元素的质量比为
39:127:48
39:127:48
.(3)服用碘片治疗131I辐射的推荐服用剂量是每日摄入KI为130-170mg,假设服用某碘片每日补充166mg KI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
5
5
kg.分析:(1)根据在化合物中正负化合价代数和为零,结合碘酸钾(KIO3)的化学式进行解答本题.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,计算出166mgKI中含有碘元素的质量;由已知每千克某品牌碘盐中KIO3的加入量为42.8mg,计算出含有碘元素的质量,进而根据题意计算每日需食用该食盐的质量.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,计算出166mgKI中含有碘元素的质量;由已知每千克某品牌碘盐中KIO3的加入量为42.8mg,计算出含有碘元素的质量,进而根据题意计算每日需食用该食盐的质量.
解答:解:(1)钾元素显+1价,氧元素显-2价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则x=+5价.
(2)碘酸钾(KIO3)中K、I、O 三种元素的质量比为39:127:(16×3)=39:127:48.
(3)166mgKI中含有碘元素的质量为:166mg×
×100%=127mg;
已知每千克某品牌碘盐中KIO3的加入量为42.8mg,含碘元素的质量为:42.8mg×
×100%=25.4mg;
如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
×1kg=5kg.
故答案为:(1)+5;(2)39:127:48;(3)5.
(2)碘酸钾(KIO3)中K、I、O 三种元素的质量比为39:127:(16×3)=39:127:48.
(3)166mgKI中含有碘元素的质量为:166mg×
| 127 |
| 39+127 |
已知每千克某品牌碘盐中KIO3的加入量为42.8mg,含碘元素的质量为:42.8mg×
| 127 |
| 39+127+16×3 |
如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
| 127mg |
| 25.4mg |
故答案为:(1)+5;(2)39:127:48;(3)5.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、有关化学式的计算并能灵活运用是正确解答的关键.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
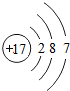
 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.为避免核辐射,需一次性口服100毫克不具放射性的碘原子(碘-127),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.请回答:
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.为避免核辐射,需一次性口服100毫克不具放射性的碘原子(碘-127),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.请回答: