题目内容
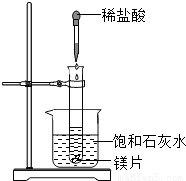
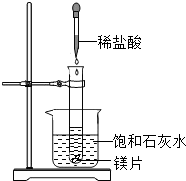 向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如右图所示.请回答:
向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如右图所示.请回答:
(1)实验中观察到的明显现象有:①剧烈反应,______;②镁条逐渐溶解;③澄清石灰水溶液变浑浊.
(2)产生上述现象③的原因是:
①______;
②______.
解:(1)由于镁与盐酸反应生成氯化镁和氢气,所以现象中有气泡产生;
(2)由于镁与盐酸反应放出热量使石灰水的温度升高,而氢氧化钙的溶解度随温度的升高减小,溶解度减小了,就溶解不了哪些溶质了,所以会析出晶体,
故答案为:(1)产生气泡;(2)①镁与盐酸反应放出热量使石灰水的温度升高;②氢氧化钙的溶解度随温度的升高减小,所以会析出晶体.
分析:(1)根据镁与盐酸反应的生成物和放热情况、氢氧化钙的溶解度与温度的关系考虑;(2)根据氢氧化钙的溶解度随温度的变化情况考虑.
点评:解答本题关键是要根据反应的生成物和反应物的状态、颜色的不同来考虑实验现象,知道金属与酸反应放出热量;知道氢氧化钙的溶解度随温度的升高减小.
(2)由于镁与盐酸反应放出热量使石灰水的温度升高,而氢氧化钙的溶解度随温度的升高减小,溶解度减小了,就溶解不了哪些溶质了,所以会析出晶体,
故答案为:(1)产生气泡;(2)①镁与盐酸反应放出热量使石灰水的温度升高;②氢氧化钙的溶解度随温度的升高减小,所以会析出晶体.
分析:(1)根据镁与盐酸反应的生成物和放热情况、氢氧化钙的溶解度与温度的关系考虑;(2)根据氢氧化钙的溶解度随温度的变化情况考虑.
点评:解答本题关键是要根据反应的生成物和反应物的状态、颜色的不同来考虑实验现象,知道金属与酸反应放出热量;知道氢氧化钙的溶解度随温度的升高减小.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
 8、向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:
8、向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答: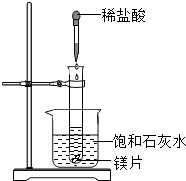 图所示,向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(20℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:
图所示,向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(20℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答: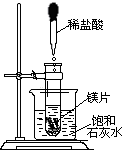 (2005?镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:
(2005?镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答: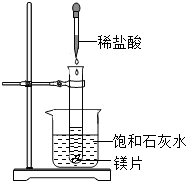 向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如右图所示.请回答:
向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如右图所示.请回答: