题目内容
【题目】(10分)定量测定是化学实验中常用的一种方法,以下是某化学兴趣小组所做的两个定量测定的实验,请回答相关问题。
【实验目的】1.测定石灰石和稀盐酸反应所生成二氧化碳的质量。
2.测定空气中氧气的体积分数。
【实验设计】实验一:测定生成二氧化碳的质量(如图1)
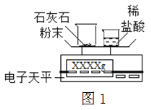
(1)写出实验中产生二氧化碳的反应文字表达式
(2)将小烧杯中的所有稀盐酸(稍过量)分几次加入到大烧杯中,并不断搅拌,判断碳酸钙完全反应的主要现象是
实验二:测定空气中氧气的体积分数(如图2)
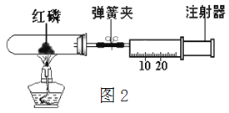
步骤:①测量试管的容积为50mL;
②……;
③装入药品,将注射器活塞调整到合适位置,连接仪器;
④用弹簧夹夹紧胶皮管,加热红磷(足量,且体积忽略不计),观察现象;
⑤燃烧结束后,等试管完全冷却至室温时打开弹簧夹,观察注射器活塞的移动情况。
(3)步骤②是: 。
(4)红磷燃烧的文字表达式为 ,在试管内观察到的现象是 。
(5)若实验二在打开弹簧夹前,活塞起始刻度为15mL,理论上最终注射器活塞将停留在 mL刻度处。
【数据分析及处理】
(6)已知实验一反应前的总质量[m(大烧杯+石灰石)+ m(小烧杯+稀盐酸)],要计算生成二氧化碳的质量,至少还需要的数据是 (填字母)
A. m(小烧杯) B. m(大烧杯) C. m(大烧杯+反应后剩余物)
(7)在实验二中,同学们所有的操作皆正确,但注射器活塞最终都停留在理论位置的右边,且偏差较大,造成这种误差的原因主要是 。
【答案】(1)碳酸钙+盐酸→氯化钙+水+二氧化碳
(2)加入稀盐酸以后没有气泡冒出。(其它合理的也给分)
(3)检查装置的气密性
(4)磷+氧气![]() 五氧化二磷 ;黄色火焰,大量白烟
五氧化二磷 ;黄色火焰,大量白烟
(5)5或4.5
(6)AC
(7)注射器的活塞和内壁有较大的摩擦力(合理即可)。
【解析】
试题分析:(1)石灰石与稀使用反应生成的氯化钙、水和二氧化碳:碳酸钙+盐酸→氯化钙+水+二氧化碳;
(2)碳酸钙与稀盐酸反应会产生大量的气泡,当它们完全反应时没有气泡产生;
(3)装药品前要检查装置的气密性,防止装置漏气导致测定的氧气的含量偏低;
(4)红磷燃烧产生大量的白烟:磷+氧气![]() 五氧化二磷 ;
五氧化二磷 ;
(5)氧气约占空气总体积的1/5,空气的体积是50ml ,那么氧气的体积为10ml,故打开弹簧夹后活塞向左推进10ml,即停留在5ml的位置;
(1)石灰石与稀使用反应生成的氯化钙、水和二氧化碳,二氧化碳会逸散到空气中,要知道生成的二氧化碳的质量,那么要增大小烧杯的质量和(大烧杯+反应后剩余物)的质量,即选AC;
(6)由于氧气不能完全消耗掉且注射器的活塞和内壁有较大的摩擦力,故测得的氧气的体积会偏小。

【题目】从微观的视角认识物质,对下列事实或现象的解释正确的是
事 实 | 解 释 | |
A. | 在校园内远远就能闻到桂花的香味 | 分子是随风而动的 |
B. | 水蒸发为水蒸气 | 分子之间间隔变大 |
C. | 电解水生成氢气和氧气 | 分子和原子都发生了改变 |
D. | 50mL水和50mL酒精混合后小于100mL | 混合后分子体积变小了 |

