题目内容
【题目】钢铁是使用最多的金属材料。
(1)利用新技术能将不锈钢加工成柔软的金属丝,用它和棉纤维一起编织成性能优良的劳保防护服,这是利用了不锈钢的__________(填序号,下同)。
A.耐腐蚀性 B.延展性 C.导热性 D.导电性
(2)市场上有一种含铁粉的麦片,食用后在胃酸作用下将铁粉转化为人体可吸收的铁元素,这种麦片必须真空保存,原因是_____________________________。
(3)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示。下列相关判断中,正确的是____________。
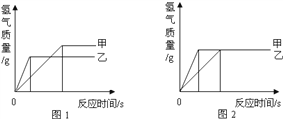
A.甲是铁,乙是锌
B.甲是锌,乙是铁
C.图1表示稀硫酸足量,图2表示稀硫酸不足量
D.图1表示金属一定有剩余,图2表示金属一定没有剩余
【答案】 AB 防止铁粉与空气中的氧气和水反应变质 AC
【解析】(1)金属具有良好的导热性、导电性、延展性等方面的性质,把金属制成合金后能够改变金属的性质,从而使得合金具有更加优良的性能;
(2)胃酸的主要成分是盐酸,能与铁反应;铁粉能与空气中的氧和水反应,使铁粉变质;
(3)根据金属活动性及酸是否足量分析。
解:(1)可以将不锈钢加工成柔软的金属丝,说明不锈钢具有良好的延展性,另外还利用了它的耐腐蚀性。故答案为:A、B;
(2)胃酸的主要成分盐酸与铁反应生成氢气,铁能与空气中的氧和水反应使铁变质。防止铁在潮湿的空气中变质,变质后的铁就不能转化为人体所需的Fe2+。
(3)锌的活动性比铁强,故甲是铁,乙是锌,所以A正确;等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,形成硫酸亚铁和硫酸锌,铁和锌的化合价相同,又铁的相对原子质量比锌小。当酸足量时,铁与酸反应时产生的气体多。当酸不足时,所含氢元素的质量相等,故产生气体的质量相等。所以C正确。