题目内容
【题目】氢氧化钠、氢氧化钙是两种常见的碱:
(1)它们有一些相似的化学性质,其原因是溶液中都含有_____。
(2)可作某些气体干燥剂的是_____。
(3)用氢氧化钙溶液检验二氧化碳,反应的化学方程式为_____。
(4)长期不合理使用化肥会使土壤酸化(如含有硝酸)熟石灰常用来改良酸性土壤,反应的化学方程式是_____。
(5)为了探究NaOH样品中是否存在NaCl、Na2CO3杂质,设计如下实验方案
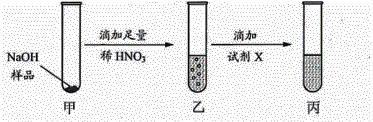
①乙中有无色无味气体产生,证明样品中含有Na2CO3.产生气体的化学方程式为_____。
②试剂X为_____溶液;可证明NaCl存在的现象是_____。
(6)化学实验活动课上,同学们进行了如图所示的实验。
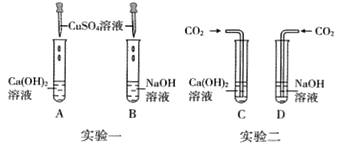
①实验一中,B试管中发生反应的化学方程式为_____。A、B两支试管中共同的实验现象是_____。
②实验二中,C试管中有白色沉淀生成,D试管中无现象。为了探究通入二氧化碳后是否发生反应,小明同学取D中少量溶液于试管中,选择合适的试剂进行实验,用化学方程式表示发生反应_____。
【答案】氢氧根离子(或OH-) 氢氧化钠固体 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2+2HNO3=Ca(NO3)2+2H2O Na2CO3+2HNO3=2NaNO3+H2O+CO2↑ 硝酸银(AgNO3)溶液 生成白色沉淀 2NaOH+CuSO4=Na2SO4+Cu(OH)2↓ 生成蓝色沉淀 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
【解析】
二氧化碳和氢氧化钙生成碳酸钙和水,氢氧化钙和硝酸反应生成硝酸钙和水,碳酸钠和稀硝酸反应生成硝酸钠、水和二氧化碳,二氧化碳和氢氧化钠反应生成碳酸钠和水,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠。
(1)氢氧化钠是氢氧根离子和钠离子构成的,氢氧化钙是由钙离子和氢氧根离子构成的,它们有一些相似的化学性质,其原因是溶液中都含有氢氧根离子(或OH-)。
(2)氢氧化钠是碱性物质,可以干燥碱性气体和中性气体,故可作某些气体干燥剂的是氢氧化钠固体。
(3)用氢氧化钙溶液检验二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙和水,反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O。
(4)氢氧化钙和硝酸反应生成硝酸钙和水,长期不合理使用化肥会使土壤酸化(如含有硝酸),熟石灰常用来改良酸性土壤,反应的化学方程式是Ca(OH)2+2HNO3=Ca(NO3)2+2H2O。
(5)①碳酸钠和稀硝酸反应生成硝酸钠、水和二氧化碳,乙中有无色无味气体产生,证明样品中含有Na2CO3。产生气体的化学方程式为Na2CO3+2HNO3=2NaNO3+H2O+CO2↑。
②氯化钠和硝酸银反应生成氯化银和硝酸钠,故试剂X为硝酸银(AgNO3)溶液溶液;可证明NaCl存在的现象是生成白色沉淀。
(6)①硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠,实验一中,B试管中发生反应的化学方程式为2NaOH+CuSO4=Na2SO4+Cu(OH)2↓。A中发生的反应是硫酸铜和氢氧化钙反应生成硫酸钙和氢氧化铜,故A、B两支试管中共同的实验现象是生成蓝色沉淀。
②二氧化碳和氢氧化钠反应生成碳酸钠和水,实验二中,C试管中有白色沉淀生成,二氧化碳和氢氧化钙生成碳酸钙和水,D试管中无现象。小明同学取D中少量溶液于试管中,选择加入的试剂为碳酸钠溶液,发生的反应为氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,方程式表示发生反应为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。

 全能练考卷系列答案
全能练考卷系列答案