题目内容
根据下列装置图填写有关空格:实验一
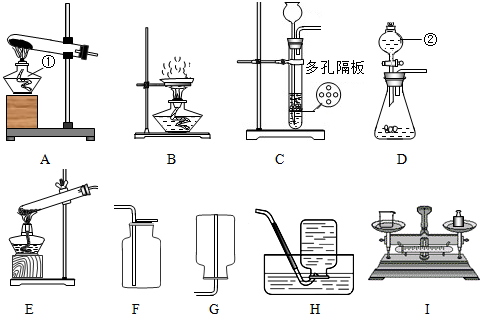
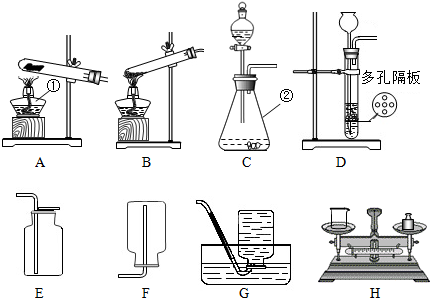
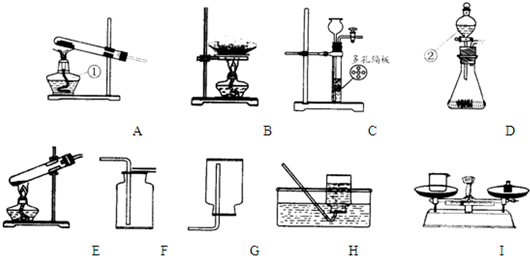
(1)装置中仪器①的名称为 ,②的名称为 .
(2)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气,同时得到氯化钙和水.通常情况下,氨气的密度比空气小且极易溶于水.若要制得干燥的氨气,则装置的连接顺序为 (填装置的编号),反应的化学方程式 .
实验二
| A | B | C | |
| 实验装置 | 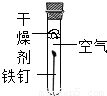 | 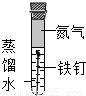 |  |
| 实验现象 | 铁钉不生锈 | 铁钉不生锈 | 铁钉生锈且水面附近锈蚀最严重 |
(1)该实验的结论是:铁生锈是铁与 等物质共同作用的结果;
(2)若在实验装置C的蒸馏水中加入少量食盐,铁片锈蚀的速率将 (填“变大”、“不变”、“变小”).
(3)实验启示:结合实验B,列举一种防止铁制品生锈的具体方法: .
【答案】分析:实验一:
(1)根据常用仪器写出仪器的名称;
(2)根据制取氨气的反应物的状态、条件和氨气的溶解性、密度判断制取和收集装置,并写出化学方程式;
实验二:
(1)钢铁生锈的条件是钢铁与氧气和水同时接触;
(2)酸性溶液、碱性溶液、盐溶液能促进金属生锈;
(3)根据实验B结合防锈方法进行解答.
解答:解:实验一:
(1)装置中仪器分别为酒精灯和分液漏斗.
(2)加热氯化铵与氢氧化钙固体混合物的方法制取氨气.是固固加热反应,我们可选用装置A作为发生装置;根据氨气密度比空气小且极易溶于水的性质可知,要用图中D向下排空气法收集.反应的化学方程式为 2NH4Cl+Ca(OH)2 CaCl2+2H2O+2NH3↑.
CaCl2+2H2O+2NH3↑.
实验二:
(1)铁生锈是铁与氧气和水的共同作用的结果;
(2)酸性溶液、碱性溶液、盐溶液能促进金属生锈,因此在实验装置C的蒸馏水中加入少量食盐,铁片锈蚀的速率将变大;
(3)防止金属生锈的方法有:在金属表面涂一层油漆;在金属表面镀一层金属等;
故答案为:
实验一:
(1)酒精灯;分液漏斗;
(2)AD;2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑;
实验二:
(1)氧气、水;
(2)变大;
(3)镀上一层金属(或刷油漆或涂油等).
点评:气体的发生装置要看反应物的状态和反应条件,气体的收集要看气体的密度和溶解性;并充分理解铁生锈是铁与水和氧气同时作用的结果,水和氧气缺少一个铁也不容易生锈.
(1)根据常用仪器写出仪器的名称;
(2)根据制取氨气的反应物的状态、条件和氨气的溶解性、密度判断制取和收集装置,并写出化学方程式;
实验二:
(1)钢铁生锈的条件是钢铁与氧气和水同时接触;
(2)酸性溶液、碱性溶液、盐溶液能促进金属生锈;
(3)根据实验B结合防锈方法进行解答.
解答:解:实验一:
(1)装置中仪器分别为酒精灯和分液漏斗.
(2)加热氯化铵与氢氧化钙固体混合物的方法制取氨气.是固固加热反应,我们可选用装置A作为发生装置;根据氨气密度比空气小且极易溶于水的性质可知,要用图中D向下排空气法收集.反应的化学方程式为 2NH4Cl+Ca(OH)2
 CaCl2+2H2O+2NH3↑.
CaCl2+2H2O+2NH3↑.实验二:
(1)铁生锈是铁与氧气和水的共同作用的结果;
(2)酸性溶液、碱性溶液、盐溶液能促进金属生锈,因此在实验装置C的蒸馏水中加入少量食盐,铁片锈蚀的速率将变大;
(3)防止金属生锈的方法有:在金属表面涂一层油漆;在金属表面镀一层金属等;
故答案为:
实验一:
(1)酒精灯;分液漏斗;
(2)AD;2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑;
实验二:
(1)氧气、水;
(2)变大;
(3)镀上一层金属(或刷油漆或涂油等).
点评:气体的发生装置要看反应物的状态和反应条件,气体的收集要看气体的密度和溶解性;并充分理解铁生锈是铁与水和氧气同时作用的结果,水和氧气缺少一个铁也不容易生锈.

练习册系列答案
相关题目