题目内容
【题目】化学兴趣小组为了测定某氧化钙变质后的成分,取该氧化钙样品10g加入103.2g稀盐酸中,恰好完全反应后得到溶液的质量为111g。请回答下列问题:
(1)实验中完全反应生成二氧化碳的质量为___________g。
(2)求样品中碳酸钙的质量分数_________。(写出计算步骤)
(3)经测定得知反应后的溶液的溶质质量分数为10%,则10g氧化钙样品中钙元素的质量为________g。
【答案】2.2 50% 4
【解析】
(1)据质量守恒定律可知,反应前后物质的总质量不变,实验中完全反应生成二氧化碳的质量为:10g+103.2g-111g=2.2g;
(2)解:设变质生成碳酸钙的质量为x
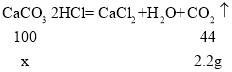
![]()
x=5 g
样品中碳酸钙的质量分数为![]()
答:样品中碳酸钙的质量分数为50%。
(3)氧化钙和水生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙,氧化钙变质的过程中涉及到的物质有氧化钙、氢氧化钙、碳酸钙;三种物质与盐酸反应后的溶液都是氯化钙溶液,故完全反应后溶液中的溶质只有CaCl2,CaCl2的质量为![]() , 根据元素守恒可知,氧化钙样品中钙元素的质量与CaCl2中钙元素的质量相等,可得氧化钙样品中钙元素的质量为
, 根据元素守恒可知,氧化钙样品中钙元素的质量与CaCl2中钙元素的质量相等,可得氧化钙样品中钙元素的质量为![]() 。
。

练习册系列答案
相关题目