题目内容
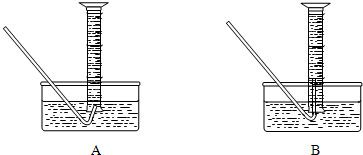
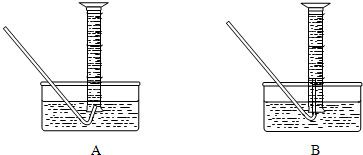
11、为了较准确测定氯酸钾完全分解产生氧气的体积,可进行以下试验:称取2.5g氯酸钾与适量二氧化锰混合,然后加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空:
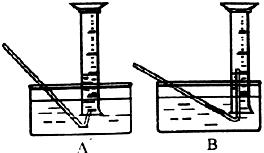
(1)测量气体体积时,可以将反应发生装置和收集装置中的气体冷却至室温再进行.则收集气体应选-上图中的
(2)若这时氧气的质量为0.98g,则使用规格的量筒(选填字母序号)
A.100mL
B.200mL
C.500mL
D.1000mL.

(1)测量气体体积时,可以将反应发生装置和收集装置中的气体冷却至室温再进行.则收集气体应选-上图中的
B
装置才合理,理由是便于量筒的移动
.(2)若这时氧气的质量为0.98g,则使用规格的量筒(选填字母序号)
D
.A.100mL
B.200mL
C.500mL
D.1000mL.
分析:(1)根据两图示中导管伸入量管中的深入浅,分析对操作产生的影响,判断所应选取的装置;
(2)计算分解0.98g氧气的体积,判断所应选用的量筒.
(2)计算分解0.98g氧气的体积,判断所应选用的量筒.
解答:解:(1)装置B中导管伸入量筒较长,便于量筒的移动,故选B装置;
(4)氧气的体积=0.96g÷1.33g/L≈0.737L=737ml
为完全收集所产生的氧气,需要使用量程大于氧气体积的量筒,故选1000mL的量筒D;
(4)氧气的体积=0.96g÷1.33g/L≈0.737L=737ml
为完全收集所产生的氧气,需要使用量程大于氧气体积的量筒,故选1000mL的量筒D;
点评:(2)题中注意把氧气的质量换算成体积,然后选用合适的量筒.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
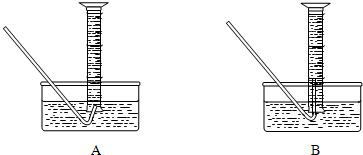
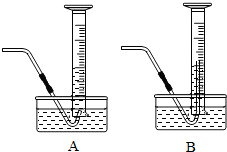 为了较准确测定氯酸钾完全分解产生氧气的体积,可进行以下试验:称取2.5g氯酸钾与适量二氧化锰混合,然后加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空:
为了较准确测定氯酸钾完全分解产生氧气的体积,可进行以下试验:称取2.5g氯酸钾与适量二氧化锰混合,然后加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空: