题目内容
蜡烛燃烧后的产物有二氧化碳和水,由质量守恒定律可知,石蜡的组成中一定含有____________、____________,可能含有____________元素。
C H O
解析试题分析:依据化学反应前后元素的种类不变可知:因为“蜡烛燃烧后生成水蒸气和二氧化碳”,则可推测水中的氢元素和二氧化碳中的碳元素都来自蜡烛,而氧元素不确定,因为氧气中也含有氧元素,要确定其是否含有氧元素得通过进一步的定量计算才能确定,所以蜡烛中一定含有碳氢两种元素,可能含有氧元素。
考点:此题考查的是质量守恒定律及其应用。
点评:本题是运用化学反应中的元素守恒思想,以及相关的融合点和嫁接点处理问题,从而培养了学生的创新思维能力。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 25、学习九年级化学上册时,同学们对蜡烛燃烧进行了探究,小华等同学意犹未尽,决定再进行进一步的探究,请你参与完成其中的一些步骤:
25、学习九年级化学上册时,同学们对蜡烛燃烧进行了探究,小华等同学意犹未尽,决定再进行进一步的探究,请你参与完成其中的一些步骤:
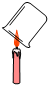
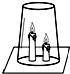
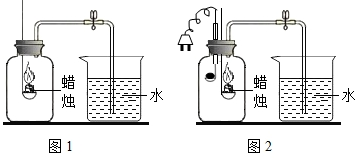
 某学习小组用如图进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某学习小组用如图进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
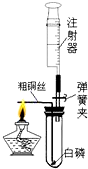 注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动:
注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动: