题目内容
运用侯氏制碱法制得的纯碱中可能含有少量氯化钠.现取某种仅含有氯化钠一种杂质的纯碱样品23.4g全部溶解在350.0g水中,再加入氯化钡溶液166.0g,恰好完全反应生成碳酸钡沉淀.过滤出沉淀并干燥后,称得沉淀的质量为39.4g.
(1)求23.4g纯碱样品中碳酸钠的质量.
(2)求滤液中氯化钠的质量分数.
解:设原混合物中碳酸钠的质量是x;生成的氯化钠的量为y
则有:Na2CO3+BaCl2=BaCO3↓+2NaCl
106 197 117
x 39.4 y
106:197=x:39.4 解得x=21.2g 197:117=39.4:y 解得y=23.4g
反应后溶液中溶质的质量分数为: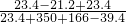 ×100%=5.12%
×100%=5.12%
答:(1)原混合物中碳酸钠的量是21.2g
(2)反应后溶质的质量分数为5.12%
分析:根据化学方程式的计算,利用沉淀的量求反应物碳酸钠的量,利用原来氯化钠的质量加上生成的量,求滤液中的总量,溶液的量可通过反应前物质的总和减生成沉淀的量得到.
点评:此题考查的是利用化学方程式的计算,这种问题首先要分析里面发生的反应,找到已知量,利用已知量再求未知量.
则有:Na2CO3+BaCl2=BaCO3↓+2NaCl
106 197 117
x 39.4 y
106:197=x:39.4 解得x=21.2g 197:117=39.4:y 解得y=23.4g
反应后溶液中溶质的质量分数为:
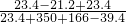 ×100%=5.12%
×100%=5.12%答:(1)原混合物中碳酸钠的量是21.2g
(2)反应后溶质的质量分数为5.12%
分析:根据化学方程式的计算,利用沉淀的量求反应物碳酸钠的量,利用原来氯化钠的质量加上生成的量,求滤液中的总量,溶液的量可通过反应前物质的总和减生成沉淀的量得到.
点评:此题考查的是利用化学方程式的计算,这种问题首先要分析里面发生的反应,找到已知量,利用已知量再求未知量.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目