题目内容
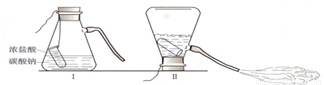
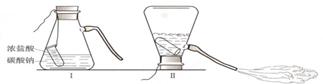
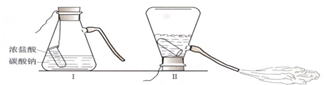 探究泡沫灭火器原理的实验时,小东不小心把喷出的泡沫液体喷到小明的衣服上,当时来不及清洗,下课后发现衣服上有点点白斑,这种白色固体的组成可能是
探究泡沫灭火器原理的实验时,小东不小心把喷出的泡沫液体喷到小明的衣服上,当时来不及清洗,下课后发现衣服上有点点白斑,这种白色固体的组成可能是A
A
A.氯化钠 B.盐酸 C.氢氧化钠 D.
碳酸钠
碳酸钠
.分析:根据盐酸与碳酸钠反应的生成物和反应物是否过量考虑.
解答:解:由于碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,所以白色固体中含有氯化钠,如果恰好完全反应,白色固体是氯化钠,如果碳酸钠过量时,白色固体中还含有碳酸钠,因为碳酸钠属于白色固体,如果盐酸过量时盐酸中溶质是氯化氢,不是白色固体,所以白色固体可能的组成是可能含有碳酸钠.
故答案为:A;碳酸钠.
故答案为:A;碳酸钠.
点评:判断反应完的溶质组成时,要考虑两个方面:一是看生成物,二是看反应物是否过量.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
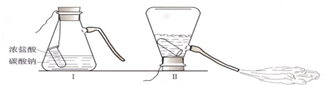 探究泡沫灭火器原理的实验时,小东不小心把喷出的泡沫液体喷到小明的衣服上,当时来不及清洗,下课后发现衣服上有点点白斑,这种白色固体的组成可能是________
探究泡沫灭火器原理的实验时,小东不小心把喷出的泡沫液体喷到小明的衣服上,当时来不及清洗,下课后发现衣服上有点点白斑,这种白色固体的组成可能是________