题目内容
潜水员的呼吸面具用Na2O2与人体呼出的CO2反应来制取氧气,供潜水员呼吸,其化学反应为:2Na2O2+2CO2═2x+O2
(1)试推断X的化学式______
(2)39克Na2O2完全反应,可放出O2______克.
解:(1)据质量守恒定律,在反应前后各元素原子的个数不变.从2Na2O2+2CO2=2x+O2看,钠原子反应前共有4个,反应后除x外没有,所以2x中有4个,从而x中有2个钠原子;氧原子反应前共有8个,反应后除x外有2个,故2x里有6个,从而得出x里有3个;碳原子反应前有2个,反应后除x外没有,故2x里有2个,从而得出x里有1个碳原子,所以x的化学式为Na2CO3.
(2)设生成氧气的质量为x,
2Na2O2+2CO2=2Na2CO3+O2
156 32
39g x
 =
=
解得:x=8g,
故答案为:(1)Na2CO3;(2)8.
分析:(1)根据质量守恒定律的实质,化学反应前后原子的种类和数目不变求出化学式.
(2)由过氧化钠的质量根据化学方程式可以计算出生成氧气的质量.
点评:在推断物质的化学式时,一定要注意x前是否有化学计量数.
(2)设生成氧气的质量为x,
2Na2O2+2CO2=2Na2CO3+O2
156 32
39g x
 =
=
解得:x=8g,
故答案为:(1)Na2CO3;(2)8.
分析:(1)根据质量守恒定律的实质,化学反应前后原子的种类和数目不变求出化学式.
(2)由过氧化钠的质量根据化学方程式可以计算出生成氧气的质量.
点评:在推断物质的化学式时,一定要注意x前是否有化学计量数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 铜质奖牌 B.
铜质奖牌 B. 铜导线 C.
铜导线 C. 铜火锅
铜火锅
 2CuSO4+2H2O
2CuSO4+2H2O 甲、乙两种固体物质的溶解度曲线如图所示:
甲、乙两种固体物质的溶解度曲线如图所示:
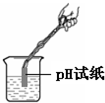
 蒸发食盐水
蒸发食盐水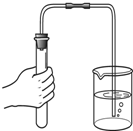 检查装置气密性
检查装置气密性