题目内容
(2013?大连)用以下装置进行气体的实验室抽取和性质实验.
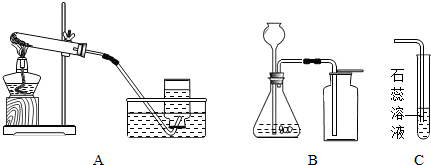
(1)选择装置A用氯酸钾和二氧化锰制氧气的化学方程式为
(2)用装置B制二氧化碳的化学方程式为
(3)将二氧化碳通入装置C中,紫色石蕊溶液变红的原因用化学方程式表示为

(1)选择装置A用氯酸钾和二氧化锰制氧气的化学方程式为
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
,用排水法收集氧气的依据是
| ||
| △ |
氧气不易溶于水
氧气不易溶于水
.(2)用装置B制二氧化碳的化学方程式为
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
,检验二氧化碳已收集满的方法是带火星的木条放在瓶口,若熄灭证明已满
带火星的木条放在瓶口,若熄灭证明已满
,长颈漏斗末端位于液面下的原因是形成液封防止气体从长颈漏斗口逸出
形成液封防止气体从长颈漏斗口逸出
.(3)将二氧化碳通入装置C中,紫色石蕊溶液变红的原因用化学方程式表示为
H2O+CO2═H2CO3
H2O+CO2═H2CO3
.分析:(1)根据加热氯酸钾和二氧化锰的混合物制取氧气,反应产生氯化钾和氧气,二氧化锰作物催化剂,写出反应的方程式;根据氧气的溶解性分析用排水法收集的原因;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式;检验CO2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,看木条是否熄灭;根据使用长颈漏斗的注意事项分析长颈漏斗末端位于液面下的原因;
(3)根据紫色石蕊溶液变红的原因是遇到了酸性物质,分析二氧化碳和水作用产生碳酸来回答.
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式;检验CO2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,看木条是否熄灭;根据使用长颈漏斗的注意事项分析长颈漏斗末端位于液面下的原因;
(3)根据紫色石蕊溶液变红的原因是遇到了酸性物质,分析二氧化碳和水作用产生碳酸来回答.
解答:解:(1)加热氯酸钾和二氧化锰的混合物制取氧气,反应产生氯化钾和氧气,二氧化锰作物催化剂,反应的方程式为:2KClO3
2KCl+3O2↑;
因为氧气不易溶于水,故可以采用排水法收集;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
检验CO2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,若木条熄灭,说明收集满;
长颈漏斗末端位于液面下的原因是:形成液封防止气体从长颈漏斗口逸出而收集不到气体;
(3)因为二氧化碳和水反应产生碳酸,显酸性能够使紫色的石蕊试液变成红色.
故答案为:(1)2KClO3
2KCl+3O2↑;氧气不易溶于水
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;带火星的木条放在瓶口,若熄灭证明已满;形成液封防止气体从长颈漏斗口逸出;
(3)H2O+CO2═H2CO3.
| ||
| △ |
因为氧气不易溶于水,故可以采用排水法收集;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
检验CO2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,若木条熄灭,说明收集满;
长颈漏斗末端位于液面下的原因是:形成液封防止气体从长颈漏斗口逸出而收集不到气体;
(3)因为二氧化碳和水反应产生碳酸,显酸性能够使紫色的石蕊试液变成红色.
故答案为:(1)2KClO3
| ||
| △ |
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;带火星的木条放在瓶口,若熄灭证明已满;形成液封防止气体从长颈漏斗口逸出;
(3)H2O+CO2═H2CO3.
点评:本题考查了常见气体的反应原理的书写及收集、验满、性质等的考查,属于基础性的考查,这也是中考的一个考点,要求学生要熟练掌握.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目