题目内容
【题目】【2014年四川省达州市】化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:
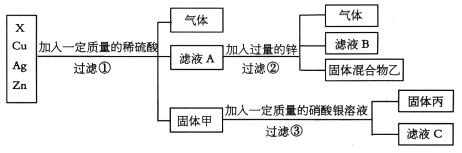
请回答:
(1)四种金属的活动性顺序由强到弱的是 ;
(2)固体丙中一定含有的金属是 ;
(3)写出③中反应的化学方程式 ;
(4)为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子 。
【答案】(1)Zn、X、Cu、Ag ;
(2)Ag ;
(3)Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)Ag+、Cu2+
【解析】
试题分析:(1)由流程可知,锌能与滤液A反应得到滤液B,而铜和银在固体甲中,故X在滤液A中,且能被锌置换,故四种金属的活动性顺序由强到弱的是Zn、X、Cu、Ag ;
(2)因为铜和银在固体甲中,且铜能与硝酸银反应,所以固体丙中一定含有的金属是银;
(3)③发生的反应是铜和硝酸银生成硝酸铜和银,反应的化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)加入稀盐酸有白色沉淀产生,则滤液中含有Ag+,又因为反应③为铜和硝酸银生成硝酸铜和银,则滤液C中一定含有的阳离子Ag+、Cu2+。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目