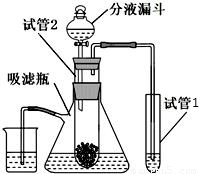
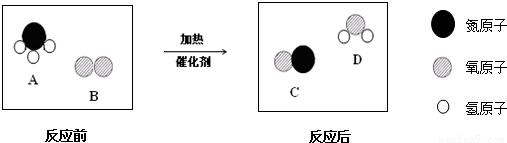
题目内容
(2011?房山区一模)学好化学可以避免生活中的盲目行为.日本大地震造成的核泄露事故使“防辐射”成为热点话题,“吃碘防辐射”之说等原因在社会上造成短暂的“盐荒”(“盐王爷”风波).右表是某地市场被抢购的一种“加碘食盐”包装袋上的部分说明.配制该产品时每袋产品中最多加入碘酸钾( )| 规格 | 250g/袋 |
| 配料 | 氯化钠、碘酸钾 KIO3 |
| 含碘量 | (20~30mg)/1kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏方法 | 避光、避热、密封、防潮 |
【答案】分析:根据标签中含碘量(20-30mg)/1Kg及规格250g/袋,可求得该袋食盐中含碘元素的质量,然后由配料:氯化钠、碘酸钾(KIO3)可得知食盐中的碘元素都含有碘酸钾中,利用碘酸钾中碘元素的质量分数,可计算该袋食盐中所含碘酸钾的最大值.
解答:解:该袋加碘食盐中最多含碘元素的质量=250g÷1000×30mg/1Kg=7.5mg
配制该产品时每袋产品中最多加入碘酸钾的质量=7.5mg÷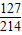 ×100%=12.6mg
×100%=12.6mg
故选A.
点评:根据计算的需要自行在标签中挑选所需要数据,使得本题具有一定的难度,相当于自己编写题目.
解答:解:该袋加碘食盐中最多含碘元素的质量=250g÷1000×30mg/1Kg=7.5mg
配制该产品时每袋产品中最多加入碘酸钾的质量=7.5mg÷
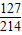 ×100%=12.6mg
×100%=12.6mg故选A.
点评:根据计算的需要自行在标签中挑选所需要数据,使得本题具有一定的难度,相当于自己编写题目.

练习册系列答案
相关题目
(2011?房山区一模)化学实验小组的同学要测定从商店买来的某品牌纯碱中碳酸钠的质量分数(已知杂质为NaCl),经过讨论,他们设计并进行了如下实验(反应过程中不考虑水和氯化氢的挥发):
取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
(1)第______次加入稀盐酸后样品完全反应.
(2)请你帮助他们计算出样品中碳酸钠的质量分数.
(3)求样品与稀盐酸恰好完全反应时所得溶液中溶质的质量分数.
取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.90 | 97.80 | 116.70 | 135.60 | 155.05 | 175.05 | 195.05 |
(2)请你帮助他们计算出样品中碳酸钠的质量分数.
(3)求样品与稀盐酸恰好完全反应时所得溶液中溶质的质量分数.