题目内容
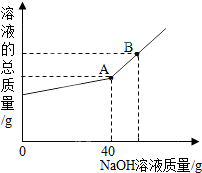 在一烧杯中盛有一定质量的金属镁,向其中加入足量的稀硫酸,至恰好完全反应,在一定温度下得到40g MgSO4的不饱和溶液.向所得溶液中逐滴滴入溶质质量分数为10%的NaOH溶液,溶液的总质量与滴入NaOH溶液的质量的质量关系曲线如图所示.请根据题意回答下列问题:
在一烧杯中盛有一定质量的金属镁,向其中加入足量的稀硫酸,至恰好完全反应,在一定温度下得到40g MgSO4的不饱和溶液.向所得溶液中逐滴滴入溶质质量分数为10%的NaOH溶液,溶液的总质量与滴入NaOH溶液的质量的质量关系曲线如图所示.请根据题意回答下列问题:(1)写出在整个实验过程中观察到的一项实验现象
(2)当滴入过量NaOH溶液至图中B点时,烧杯中溶液里含有的溶质为
(3)当滴入10%的NaOH溶液40g时(即图中A点),恰好完全反应.试通过计算,求此时烧杯中所得不饱和溶液的质量(计算结果精确到0.1g)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据MgSO4与NaOH反应的情况进行分析;
(2)由图示数据可知,当滴入NaOH溶液至图中B点时,硫酸镁完全反应,氢氧化钠过量,据此分析;
(3)当滴入NaOH溶液至A点时,恰好完全反应.利用硫酸镁与氢氧化钠反应的化学方程式和氢氧化钠的质量,列出比例式,就可计算出生成沉淀的质量,然后根据“所得不饱和溶液的质量=参与反应的溶液质量-生成沉淀质量”计算.
(2)由图示数据可知,当滴入NaOH溶液至图中B点时,硫酸镁完全反应,氢氧化钠过量,据此分析;
(3)当滴入NaOH溶液至A点时,恰好完全反应.利用硫酸镁与氢氧化钠反应的化学方程式和氢氧化钠的质量,列出比例式,就可计算出生成沉淀的质量,然后根据“所得不饱和溶液的质量=参与反应的溶液质量-生成沉淀质量”计算.
解答:解:(1)MgSO4与NaOH反应的观察到的明显实验现象是:有白色沉淀生成;
故答案为:有白色沉淀生成;
(2)当滴入NaOH溶液时,氢氧化钠与硫酸镁发生反应,化学方程式为:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,由图示数据可知,至图中B点时,硫酸镁完全反应,氢氧化钠过量,故此时烧杯中溶液里含有的溶质是Na2SO4和NaOH;
故答案为:Na2SO4、NaOH;
(3)解:40g10%的NaOH溶液中含NaOH的质量是:40g×10%=4g;
设反应中生成Mg(OH)2的质量为x,
CuSO4+2NaOH═Mg(OH)2↓+Na2SO4
80 58
4g x
=
x=2.9g
烧杯里所得不饱和溶液的质量为:40g+40-2.9g=77.1g.
答:此时烧杯中所得不饱和溶液的质量为77.1g.
故答案为:有白色沉淀生成;
(2)当滴入NaOH溶液时,氢氧化钠与硫酸镁发生反应,化学方程式为:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,由图示数据可知,至图中B点时,硫酸镁完全反应,氢氧化钠过量,故此时烧杯中溶液里含有的溶质是Na2SO4和NaOH;
故答案为:Na2SO4、NaOH;
(3)解:40g10%的NaOH溶液中含NaOH的质量是:40g×10%=4g;
设反应中生成Mg(OH)2的质量为x,
CuSO4+2NaOH═Mg(OH)2↓+Na2SO4
80 58
4g x
| 80 |
| 58 |
| 4g |
| x |
x=2.9g
烧杯里所得不饱和溶液的质量为:40g+40-2.9g=77.1g.
答:此时烧杯中所得不饱和溶液的质量为77.1g.
点评:本题主要考查学生利用化学方程式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的用途中,主要利用其物理性质的是( )
| A、焊接金属时用氮气做保护气 |
| B、用生石灰做干燥剂 |
| C、用铜制作导线 |
| D、用二氧化碳灭火器灭火 |
分类是学习和研究物质的一种常见的方法,下列物质的分类正确的是( )
| A、臭氧中只含氧元素,属于单质 |
| B、高锰酸钾中含有氧元素,属于氧化物 |
| C、硫酸钾中含有硫酸根离子,属于酸 |
| D、碳酸钙中含有碳元素,属于有机物 |
生活中处处有化学,下列生活中的做法合理的是( )
| A、用石墨除去冰箱中的异味 |
| B、用食盐水浸泡菜刀,可防止菜刀生锈 |
| C、利用洗洁精对油污的乳化作用清洁锅碗瓢盆 |
| D、用厨房清洁剂除去水壶内的水垢 |