题目内容
【题目】现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
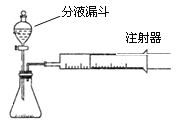
(1)下列方法能检查该装置气密性的是______。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)MnO2催化下H2O2分解的化学方程式是 。
(3)甲小组有如下实验设计方案,完成下表。
实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 探究对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
(4)甲、乙两小组得出如图数据。
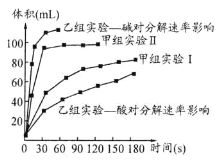
甲组实验得出的数据可知:浓度越大,H2O2分解速率 ;
由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下, H2O2在 (填“酸”或“碱”)性环境下放出气体速率较快;乙组提出可以用Ba O2固体与硫酸溶液反应制H2 O2(已知还生成硫酸钡沉淀),其化学反应方程式为 ;支持这一方案的理是 。
【答案】(1)AB;(2)2H2O2![]() 2H2O+O2↑;(3)浓度;
2H2O+O2↑;(3)浓度;
(4)①越快;②碱; BaO2 +H2SO4= BaSO4 ↓+H2O2; 过氧化氢在酸性环境下分解较慢
【解析】
试题分析:(1)气密性检验遵循的原则是先让装置和水形成封闭的体系,然后改变某一条件使压强发生变化来判断气密性的好坏。A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差,正确;B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移,停止加热后注射器活塞回到原来位置,则气密性良好,反之,气密性差,正确;C、由B分析可知,错误。故选AB(2)MnO2催化下H2O2分解的化学方程式是2H2O2![]() 2H2O+O2↑;(3)根据表格内容可知,该实验是为了探究浓度对过氧化氢分解速率的影响;(4)甲组实验得出的数据可知:浓度越大,H2O2分解速率越快;由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下, H2O2在碱性环境下放出气体速率较快;根据题目信息知,化学方程式为:BaO2 +H2SO4= BaSO4 ↓+H2O2;支持这一方案的理由是过氧化氢在酸性环境下分解较慢
2H2O+O2↑;(3)根据表格内容可知,该实验是为了探究浓度对过氧化氢分解速率的影响;(4)甲组实验得出的数据可知:浓度越大,H2O2分解速率越快;由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下, H2O2在碱性环境下放出气体速率较快;根据题目信息知,化学方程式为:BaO2 +H2SO4= BaSO4 ↓+H2O2;支持这一方案的理由是过氧化氢在酸性环境下分解较慢