题目内容
【题目】某碳酸钠样品中含有少量氯化钠,现取样品13.9g,加入66.1g水配成溶液,再加入80g氯化钙溶液,恰好完全反应,过滤后得到滤液150g,求反应后所得溶液的溶质质量分数。
【答案】10%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了碳酸钙,所以可以求算碳酸钙的质量,根据碳酸钙的质量和对应的化学方程式求算碳酸钠以及生成的氯化钠的质量,进而求算对应的质量分数。
根据质量守恒定律可得,生成的碳酸钙的质量为13.9g+66.1g+80g-150g=10g
设碳酸钠的质量为x,生成的氯化钠的质量为y
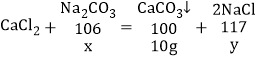
![]()
x=10.6g
y=11.7g
反应后所得溶液的溶质质量分数为![]() ×100%=10%
×100%=10%
答:反应后所得溶液的溶质质量分数为10%。

练习册系列答案
相关题目