题目内容
【题目】写出下列反应的化学方程式,并按要求填空。
(1)工业上用一氧化碳和赤铁矿(主要成分是三氧化二铁)在高温下炼铁:__________。
(2)生石灰作为干燥剂: ____________________,该反应属于_________ (选填“放或吸热”)。
(3)用氢氧化钠溶液吸收少量二氧化硫气体:___________________________________。
(4)用稀硫酸除去铁锈:_____________________,反应后所得溶液的颜色为_________色。
(5)硫酸铵固体和氢氧化钙固体混合研磨:___________,该反应的基本反应类型是_______。
(6)生成沉淀的中和反应:_________________________________,恰好完全反应后液体的导电性比反应前的______ (选填“增强”、“减弱”或“不变”)。
【答案】 Fe2O3+3CO ![]() 2Fe+3CO2 CaO+H2O==Ca(OH)2 放热 2NaOH + CO2=== Na2CO3 + H2O Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O 黄 (NH4)2SO4 + Ca(OH)2 == CaSO4 + 2H2O + 2NH3↑ 复分解反应 H2SO4 + Ba(OH)2 == BaSO4↓+ 2H2O 减弱
2Fe+3CO2 CaO+H2O==Ca(OH)2 放热 2NaOH + CO2=== Na2CO3 + H2O Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O 黄 (NH4)2SO4 + Ca(OH)2 == CaSO4 + 2H2O + 2NH3↑ 复分解反应 H2SO4 + Ba(OH)2 == BaSO4↓+ 2H2O 减弱
【解析】(1)工业上用一氧化碳和赤铁矿在高温下炼铁的化学方程式为:Fe2O3+3CO ![]() 2Fe+3CO2 (2)生石灰能与水反应,可作为干燥剂,CaO+H2O==Ca(OH)2,该反应放出大量的热。(3)氢氧化钠溶液能与二氧化硫气体反应生成亚硫酸钠和水。(4)铁锈主要成分是氧化铁,能与稀硫酸反应,生成黄色的硫酸铁溶液。(5)铵盐能与碱反应生成氨气、水、盐,盐与酸之间的反应属于复分解反应。(6)中和反应生成盐和水,BaSO4沉淀不导电,水几乎不导电,所以反应后导电性减弱。
2Fe+3CO2 (2)生石灰能与水反应,可作为干燥剂,CaO+H2O==Ca(OH)2,该反应放出大量的热。(3)氢氧化钠溶液能与二氧化硫气体反应生成亚硫酸钠和水。(4)铁锈主要成分是氧化铁,能与稀硫酸反应,生成黄色的硫酸铁溶液。(5)铵盐能与碱反应生成氨气、水、盐,盐与酸之间的反应属于复分解反应。(6)中和反应生成盐和水,BaSO4沉淀不导电,水几乎不导电,所以反应后导电性减弱。

【题目】氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示,请结合图表数据回答下列问题:
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |
(1)下图表示________(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
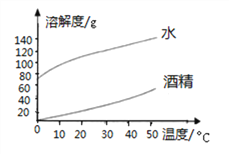
(2)温度从20℃升到40℃时,氢氧化钠在水中的溶解度变化__________(填“大于”或“小于”)碳酸钠在水中的溶解度变化。
(3)40℃ 时,若将50gNaOH分别投入到100g水和100g酒精中,能形成饱和溶液的溶剂是__,再将CO2通入所得NaOH的酒精溶液中,观察到的现象为______________。
(4)若要对比两种固体物质的溶解性,必须在_____________、______________ 、_____________的条件下进行对比。
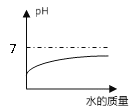
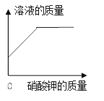
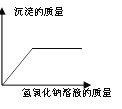
【题目】下列四个图像中,不能正确表示对应变化关系的是 ( )
|
|
|
|
A.向一定量稀硫酸中加水稀释 | B.一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | C.加热一定质量的 高锰酸钾固体 | D.向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液 |
A. A B. B C. C D. D
【题目】如图是一套检验气体性质的实验装置,向装置中持续通入气体X,若打开活塞K,只观察到紫色石蕊变红;若关闭活塞K,可观察到紫色石蕊试液变红,澄清石灰水变浑浊。据此判断气体X和洗瓶内的液体Y可能是( )
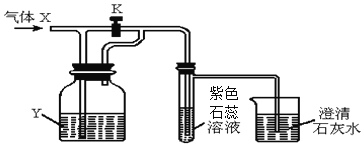
A | B | C | D | |
X | 二氧化碳 | 氯化氢 | 二氧化碳 | 氯化氢 |
Y(足量) | 水 | 碳酸钠溶液 | 氢氧化钠溶液 | 氢氧化钠溶液 |
A. A B. B C. C D. D
【题目】实验加试中同学发现:向澄清石灰水中吹入![]() ,产生白色沉淀,再不断吹入
,产生白色沉淀,再不断吹入![]() ,沉淀全部溶解。同学们对白色沉淀溶解的生成物展开如下探究:
,沉淀全部溶解。同学们对白色沉淀溶解的生成物展开如下探究:
活动一:探究白色沉淀溶解的生成物是什么?
【查阅资料】碳酸钙、水和二氧化碳反应可生成碳酸氢钙。请完成资料里所涉及的化学方程式______。
活动二:探究碳酸氢钙具有哪些化学性质?
请你就碳酸氢钙可能具有的化学性质提出两个猜想并设计实验加以验证。可供使用的试剂和仪器为:![]() 溶液、
溶液、![]() 溶液、澄清石灰水、稀盐酸、NaOH溶液、试管、烧杯、导管、玻璃棒。
溶液、澄清石灰水、稀盐酸、NaOH溶液、试管、烧杯、导管、玻璃棒。
序号 | 猜想 | 操作步骤 | 可能观察到的现象 |
一 | ___________ | ___________ | ___________ |
二 | ___________ | ___________ | ___________ |