题目内容
【题目】下列是初中化学部分重要的实验或实验装置。请按要求填空:
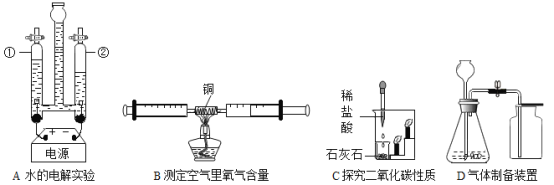
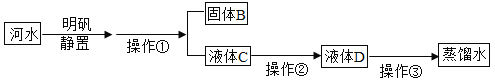
(1)A实验玻璃管②中产生的气体是_______(填名称);该气体的一种用途是_____________。
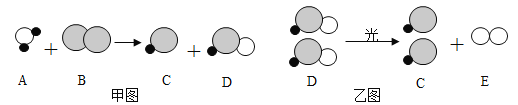
(2)B实验的产物是_______。(填化学式)
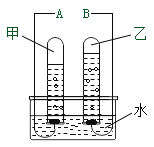
(3)C实验说明二氧化碳具有的化学性质是_____________、___________;物理性质是_________。写出该实验中的化学反应方程式_____________。
(4)若用D装置制备并收集氧气,选用的药品是__________(填名称)和二氧化锰,反应的化学方程式为_____________。
【答案】氢气 做燃料(还原剂等) CuO 不燃烧 不支持燃烧 密度比空气大 CaCO3+2HCl=CaCl2+H2O+CO2↑ 过氧化氢溶液 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
(1)电解水产生氢气和氧气,氢气和氧气的体积比为2:1,故A实验玻璃管②中产生的气体是氢气;
氢气的一种用途是做清洁燃料;
(2)B实验是铜在高温下和氧气反应生成氧化铜,故实验产物是氧化铜:CuO;
(3)C实验的现象是下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳具有的化学性质是二氧化碳不燃烧,也不支持燃烧;物理性质是二氧化碳的密度比空气大;
石灰石的主要成分是碳酸钙,和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)若用D装置制备并收集氧气,选用的药品是过氧化氢溶液和二氧化锰,二者反应生成水和氧气,反应的化学方程式为2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。

 阅读快车系列答案
阅读快车系列答案【题目】气体制取及性质验证是重要的化学实验活动,请结合下图所示实验装置,回答下列问题。
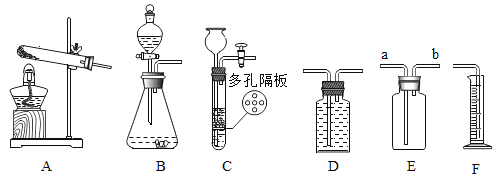
(1)用氯酸钾制氧气反应的化学方程式是_____ 选用的发生装置是_____(选填序号),用E装置瓶口向上收集氧气时,应由_____端通入(填a或b)。
(2)用B装置制取氧气。若过氧化氢和二氧化锰反应过于剧烈,在导管口不能使带火星的木条复燃,可能的原因是_____。
(3)实验室用B装置制取二氧化碳进行了如下实验研究:
实验编号 | 甲 | 乙 | 丙 | 丁 | |
药品 | 大理石 | mg;块状 | mg;块状 | mg;粉末 | mg;粉末 |
酸(过量) | wg;稀盐酸 | wg; 浓盐酸 | wg;稀盐酸 | wg; 浓盐酸 | |
①若要研究盐酸浓度大小对反应的影响,可选择实验甲与_____对照(选填实验编号)。
②除酸的浓度外,上述实验研究的另一个影响反应的因素是_____。
③研究发现酸浓度越大,反应速度越快,与甲比较,对丁分析正确的是_____(填编号)。
A 反应更为剧烈 B 更适合实验室制取二氧化碳 C 产生二氧化碳的质量更大
(4)用C装置制取气体时,块状固体放在多孔隔板上,可以使反应随时发生和停止,C装置不适用于下列哪种气体的制取:_____(填编号)。
A 锌和稀硫酸制氢气 B 大理石与稀盐酸制二氧化碳 C 过氧化氢和二氧化锰制氧气
(5)要测量收集氢气的体积,应该把发生装置C与_____连接。