题目内容
【题目】某同学在实验室发现一瓶由碳酸钠和氯化钠组成的混合溶液,为了测定该混合溶液中碳酸钠的质量分数,该同学设计了如下实验:取该混合溶液100g,向其中逐滴加入稀盐酸,当加入盐酸的质量为20g、40g、60g、80g时,生成气体的质量见下表(气体的溶解度忽略不计).
第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | |
稀盐酸的质量/g | 20 | 40 | 60 | 80 |
生成气体的质量/g | 1.8 | n | 4.4 | 4.4 |
请计算:
(1)第Ⅱ组数据n为g.
(2)混合溶液中碳酸钠的质量分数是多少?(写出计算过程,结果精确至0.1%)
【答案】
(1)3.6
(2)解:由于第一次加入盐酸生成气体是1.8g,而第三次相对假如第二次加入时每次加入20g盐酸都对应1.8g还是有气体生成的,所以可以确定第二次也是每20g盐酸生成1.8g气体,即n为3.6g.
由于最多生成了二氧化碳4.4g,设参加反应的碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+ | CO2↑ |
106 | 44 |
x | 4.4g |
![]() =
= ![]()
x=10.6g
混合溶液中碳酸钠的质量分数是 ![]() ×100%=10.6%
×100%=10.6%
【解析】解:由于第一次加入盐酸生成气体是1.8g,而第三次相对假如第二次加入时每次加入20g盐酸都对应1.8g还是有气体生成的,所以可以确定第二次也是每20g盐酸生成1.8g气体,即n为3.6g. 由于最多生成了二氧化碳4.4g,设参加反应的碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+ | CO2↑ |
106 | 44 |
x | 4.4g |
![]() =
= ![]()
x=10.6g
混合溶液中碳酸钠的质量分数是 ![]() ×100%=10.6%
×100%=10.6%
答:(1)第Ⅱ组数据n为 3.6g.(2)混合溶液中碳酸钠的质量分数是10.6%.
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
每次加盐酸前烧杯及所盛 | 158.0 | 181.2 | X | 228.6 |
所加盐酸的溶液质量/g | 25.0 | 25.0 | 25.0 | 25.0 |
充分反应后烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
每次生成的二氧化碳质量/g | 1.8 | 1.8 | Y | 0 |
(1)仔细分析表中数据,写出X、Y两数据的值:X , Y .
(2)请你通过计算说明该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%
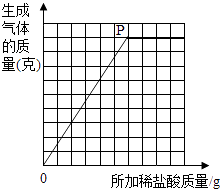
(3)根据实验数据,某同学在如图坐标纸上绘制出了所加稀盐酸质量与生成气体质量关系的曲线请你求出图中转折处P点的坐标.(保留一位小数)