题目内容
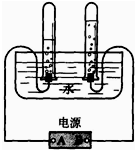
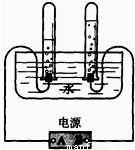
 根据图所示电解水装置中的现象,判断所接电源的正负极,图中A点表示
根据图所示电解水装置中的现象,判断所接电源的正负极,图中A点表示负
负
极,B点表示正
正
极.实验测得水分解得到氢气、氧气的体积比(标准状况)是2:1
2:1
,试根据这一数据,推算水中氢元素和氧元素的质量比为1:8
1:8
.(已知在标准状况下,氢气的密度是0.0889g/L,氧气的密度是1.43g/L).分析:根据电解水产生的氢气体积大,氧气体积小,正极产生氧气,负极产生氢气,电解水获得的实验结论,要记住.
解答:解:由正氧负氢,氢二氧一,可推出负极产生的是氢气,正极产生的是氧气,氢气和氧气的体积比为2:1,生成的氢气与氧气的质量比为:
=
.依据质量守恒定律中反应前后元素的质量不变可知水中氢氧两种元素的质量比也是:1:8.
故答案为:负;正;2:1;1:8;
| 2×0.0889 |
| 1×1.43 |
| 1 |
| 8 |
故答案为:负;正;2:1;1:8;
点评:要熟记正氧负氢,氢二氧一,依据有关的数据来计算水中氢氧元素的质量比

练习册系列答案
相关题目

 根据图所示电解水装置中的现象,判断所接电源的正负极,图中A点表示________极,B点表示________极.实验测得水分解得到氢气、氧气的体积比(标准状况)是________,试根据这一数据,推算水中氢元素和氧元素的质量比为________.(已知在标准状况下,氢气的密度是0.0889g/L,氧气的密度是1.43g/L).
根据图所示电解水装置中的现象,判断所接电源的正负极,图中A点表示________极,B点表示________极.实验测得水分解得到氢气、氧气的体积比(标准状况)是________,试根据这一数据,推算水中氢元素和氧元素的质量比为________.(已知在标准状况下,氢气的密度是0.0889g/L,氧气的密度是1.43g/L).