题目内容
【题目】汽车、电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。请回答下列有关问题:
(1)若用100g质量分数为98%的浓硫酸(密度为1.84g·cm-3)配制该稀硫酸时,需要蒸馏水(密度为1g·cm-3)的体积为 mL(精确到0.1);
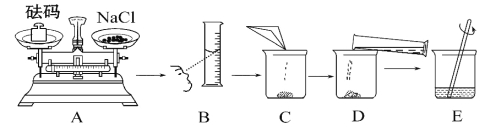
(2)该实验的主要步骤有计算、量取、稀释配制、装瓶并贴标签。请填写标签:

(3)用量筒量取浓硫酸时俯视读数,所配溶液溶质质量分数 20%(填“大于”“小于”或“等于”)。
【答案】(1)390.0 mL;(2)溶液的名称和溶质的质量分数;(3)小于
【解析】本题考查溶液的配制和溶质质量分数的相关计算,解题的关键是依据溶液稀释时稀释前后溶液中溶质的质量不变进行计算及量筒俯视读数进行误差分析。(1)解:设需要蒸馏水的体积为x,100g×98%=(100g+1g·cm-3×x)×20%,
x=390.0 mL;(2)溶液的标签应标明溶液的名称和溶质的质量分数;(3)用量筒量取浓硫酸时俯视读数,实际量取的浓硫酸的体积偏小,因此所配溶液溶质质量分数< 20%。

【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
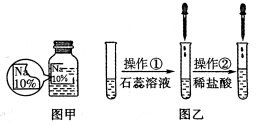
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。