题目内容
【题目】(2013安徽)以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如下:
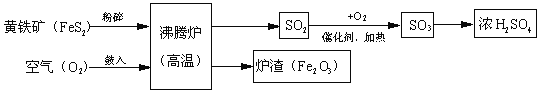
(1)写出流程图中一种氧化物的名称___________。
(2)将黄铁矿粉碎,目的是_______________________________________________。
(3)流程中SO2转化为SO3的化学方程式为_________________________________。
(4)实验室稀释浓硫酸应注意什么?______________________________________。
(5)炉渣(Fe2O3)在工业上可用来___________________________________。
【答案】(1)二氧化硫或三氧化硫或三氧化二铁。
(2)增大反应物的接触面积。
(3)2SO2+O2![]() 2SO3。
2SO3。
(4)将浓硫酸沿器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中。
(5)做冶铁原料。
【解析】
试题分析:(1)氧化物:由两种元素组成,其中一种元素是氧元素的化合物。本题中的氧化物有:二氧化硫(SO2)、三氧化硫(SO3)、三氧化二铁(Fe2O3)三种,可任选其一。
(2)在反应中,可通过增大反应物间的接触面积或提高反应物的浓度以加快反应速度,所以本题的目的是:增大反应物的接触面积。
(3)![]() 从图中可知,反应物为SO2和O2 ,反应条件为加热、有催化剂;生成物为SO3。故化学方程式为:2SO2+O2
从图中可知,反应物为SO2和O2 ,反应条件为加热、有催化剂;生成物为SO3。故化学方程式为:2SO2+O2![]() 2SO3
2SO3
(4)稀释浓硫酸时,一定要将浓硫酸缓慢倒入水中,切忌不可将水向浓硫酸中倒。因为在浓硫酸的稀释过程中,要放出大量的热可能使水沸腾,而水的密度又比浓硫酸的密度小,所以必须酸入水,否则水在上面极容易造成水沸腾而溅出伤人。搅拌的目的是加快散热。 浓硫酸注入水中,放出大量热,用玻璃棒不断搅拌,使热量迅速分散,防止液体飞溅。
(5)工业上可利用铁矿石(主要成分是Fe2O3)来冶炼钢铁。

 名校课堂系列答案
名校课堂系列答案