题目内容
 完成下列变化的化学方程式,并注明反应类型.
完成下列变化的化学方程式,并注明反应类型.①
②
③
④
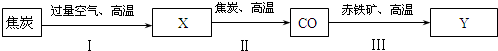
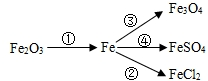
分析:①由题目中的图可知,反应物为Fe2O3、CO,生成物为Fe、CO2,反应条件为高温,故可书写化学方程式;
②由题目中的图可知,反应物为铁和盐酸,生成物为氯化亚铁和氢气,故可书写化学方程式;
③由题目中的图可知,反应物为Fe、O2,生成物为Fe3O4,反应条件为点燃,故可书写化学方程式;
④由题目中的图可知,反应物为Fe、CuSO4或硫酸,生成物为FeSO4、Cu或氢气,故可书写化学方程式.
②由题目中的图可知,反应物为铁和盐酸,生成物为氯化亚铁和氢气,故可书写化学方程式;
③由题目中的图可知,反应物为Fe、O2,生成物为Fe3O4,反应条件为点燃,故可书写化学方程式;
④由题目中的图可知,反应物为Fe、CuSO4或硫酸,生成物为FeSO4、Cu或氢气,故可书写化学方程式.
解答:解:①由题意,可知反应物、生成物、反应条件,故化学方程式为Fe2O3+3CO
2Fe+3CO2;此反应符合氧化还原反应的特点,故为氧化还原反应;
②由题意,可知反应物、生成物、反应条件,故化学方程式为Fe+2HCl═FeCl2+H2↑,此反应符合:A单质+BC→B单质+AC,故为置换反应;
③由题意,可知反应物、生成物、反应条件,故化学方程式为3Fe+2O2
Fe3O4,此反应符合:“多变一”A+B→AB,故为化合反应;
④由题意,可知反应物、生成物、反应条件,故化学方程式为Fe+CuSO4═FeSO4+Cu,此反应符合:A单质+BC→B单质+AC,故为置换反应;
故答为:①Fe2O3+3CO
2Fe+3CO2;
②Fe+2HCl═FeCl2+H2↑(置换反应);
③3Fe+2O2
Fe3O4(化合反应);
④Fe+CuSO4═FeSO4+Cu(置换反应).
| ||
②由题意,可知反应物、生成物、反应条件,故化学方程式为Fe+2HCl═FeCl2+H2↑,此反应符合:A单质+BC→B单质+AC,故为置换反应;
③由题意,可知反应物、生成物、反应条件,故化学方程式为3Fe+2O2
| ||
④由题意,可知反应物、生成物、反应条件,故化学方程式为Fe+CuSO4═FeSO4+Cu,此反应符合:A单质+BC→B单质+AC,故为置换反应;
故答为:①Fe2O3+3CO
| ||
②Fe+2HCl═FeCl2+H2↑(置换反应);
③3Fe+2O2
| ||
④Fe+CuSO4═FeSO4+Cu(置换反应).
点评:确定反应物、生成物、反应条件,正确书写化学方程式;并且掌握书写化学方程式的方法和步骤;掌握确定反应类型的方法.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目