题目内容
某气体在氧气中充分燃烧后的产物依次通过浓硫酸和氢氧化钠溶液,经完全吸收后,测得浓硫酸和氢氧化钠溶液增重的质量比为9:11,则该气体可能是
- A.CH4
- B.CH4和CO的混合气体
- C.C2H2
- D.CO和H2的混合气体
AD
分析:燃烧后的产物依次通过浓硫酸和氢氧化钠溶液,经完全吸收后,测得浓硫酸和氢氧化钠溶液增重的质量比为9:11,说明气体充分燃烧后生成水和二氧化碳且二者质量比为9:11;根据水与二氧化碳的质量比确定气体中C、H元素质量比及原子个数比,判断气体的可能组成.
解答:根据题意,气体一定含C、H元素且两元素的质量比=(11×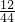 ×100%):(9×
×100%):(9×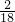 ×100%)=3:1,则气体中C、H原子个数比=
×100%)=3:1,则气体中C、H原子个数比=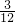 :
: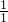 =1:4;因此该气体可能为CH4气体或CO与2H2的混合气体;
=1:4;因此该气体可能为CH4气体或CO与2H2的混合气体;
故选AD.
点评:可燃物完全燃烧时,其中C元素全部生成二氧化碳、H元素全部生成水,生成二氧化碳与水中C、H元素质量即可燃物中所含C、H元素质量.
分析:燃烧后的产物依次通过浓硫酸和氢氧化钠溶液,经完全吸收后,测得浓硫酸和氢氧化钠溶液增重的质量比为9:11,说明气体充分燃烧后生成水和二氧化碳且二者质量比为9:11;根据水与二氧化碳的质量比确定气体中C、H元素质量比及原子个数比,判断气体的可能组成.
解答:根据题意,气体一定含C、H元素且两元素的质量比=(11×
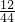 ×100%):(9×
×100%):(9×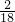 ×100%)=3:1,则气体中C、H原子个数比=
×100%)=3:1,则气体中C、H原子个数比=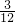 :
: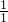 =1:4;因此该气体可能为CH4气体或CO与2H2的混合气体;
=1:4;因此该气体可能为CH4气体或CO与2H2的混合气体;故选AD.
点评:可燃物完全燃烧时,其中C元素全部生成二氧化碳、H元素全部生成水,生成二氧化碳与水中C、H元素质量即可燃物中所含C、H元素质量.

练习册系列答案
相关题目
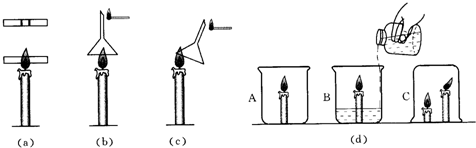

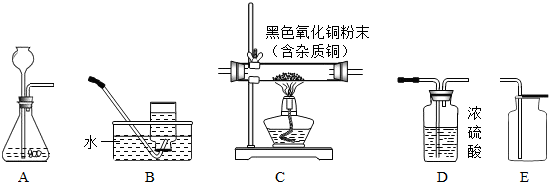
 同学们在课外活动中设计了有关气体的实验.
同学们在课外活动中设计了有关气体的实验.
