题目内容
(2012?槐荫区二模)金属是一类重要的材料,其应用十分广泛.
(1)铝的利用比铜和铁晚.金属大规模开发和利用的先后顺序与下列
A.金属的导电性 B.金属的活动性 C.金属在地壳中的含量
(2)人们常用“铜墙铁壁”来形容物体的坚固.但铁在一定条件下也能发生许多反应,如铁丝在氧气中燃烧,反应的化学方程式是
(3)制作松花蛋所用的配料主要有纯碱、生石灰、食盐、水等物质,制作时需要将它们混合并充分搅拌.请你写出制作过程中能发生的两个化学反应方程式是
(1)铝的利用比铜和铁晚.金属大规模开发和利用的先后顺序与下列
B
B
(填序号)有关. A.金属的导电性 B.金属的活动性 C.金属在地壳中的含量
(2)人们常用“铜墙铁壁”来形容物体的坚固.但铁在一定条件下也能发生许多反应,如铁丝在氧气中燃烧,反应的化学方程式是
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
.反应类型为
| ||
化合
化合
(填“分解”、“化合”、“置换”、“复分解”之一)反应.(3)制作松花蛋所用的配料主要有纯碱、生石灰、食盐、水等物质,制作时需要将它们混合并充分搅拌.请你写出制作过程中能发生的两个化学反应方程式是
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
.分析:(1)从人类大规模开发、利用金属的年限可以看出,越活泼的金属,开发利用的越晚,说明主要和金属的活动性有关;
(2)根据铁在氧气中燃烧的反应写出反应的方程式,根据反应的特点分析反应的类型;
(3)根据制取松花蛋的原料的性质分析发生的反应,写出反应的方程式.
(2)根据铁在氧气中燃烧的反应写出反应的方程式,根据反应的特点分析反应的类型;
(3)根据制取松花蛋的原料的性质分析发生的反应,写出反应的方程式.
解答:解:(1)地壳里含量最高的是金属铝,但铝开发利用的时间在铜和铁之后,说明金属大规模开发、利用的先后顺序与地壳里金属含量无关,与金属的导电性也无关.金属大规模开发利用主要和金属的活动性有关,活动性弱的金属容易以单质形式存在,易被开发和利用;活动性强的金属一般以化合物形式存在,有的还比较难冶炼;
(2)铁丝在氧气中燃烧的反应物是铁和氧气,生成物是四氧化三铁,反应条件是点燃,反应的方程式是:3Fe+2O2
Fe3O4;该反应有两种物质生成了一种物质,属于化合反应;
(3)由配料中所给的物质性质,能够发生的反应有:生石灰和水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;碳酸钠和氢氧化钙反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故答为:(1)B;(2)3Fe+2O2
Fe3O4,化合;(3)CaO+H2O═Ca(OH)2,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)铁丝在氧气中燃烧的反应物是铁和氧气,生成物是四氧化三铁,反应条件是点燃,反应的方程式是:3Fe+2O2
| ||
(3)由配料中所给的物质性质,能够发生的反应有:生石灰和水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;碳酸钠和氢氧化钙反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故答为:(1)B;(2)3Fe+2O2
| ||
点评:本题考查的知识点较多,与生活联系比较紧密.学会利用化学知识来解释、解决生活中一些问题.

练习册系列答案
相关题目
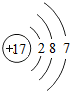 (2012?槐荫区二模)某粒子的结构示意图如图所示,下列关于该粒子的说法中,错误的是( )
(2012?槐荫区二模)某粒子的结构示意图如图所示,下列关于该粒子的说法中,错误的是( )