题目内容
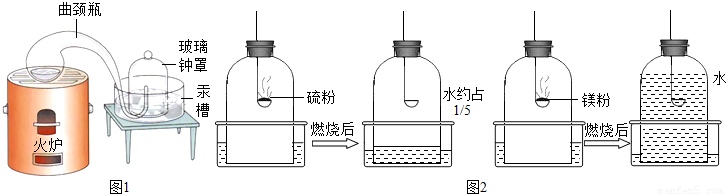
十八世纪法国化学家拉瓦锡为了研究空气的组成设计了一个划时代意义的钟罩实验(如图1),该实验证明了空气中氧气约占空气的体积
.
(1)拉瓦锡在观察到汞面浮起红色渣滓后,还继续加热12天,至红色渣滓不再增加,这样做的理由是 .
(2)拉瓦锡得到的红色渣滓是氧化汞(氧化汞的化合价为+2价),他又将氧化汞加热分解得到氧气,该反应的化学方程式是 .
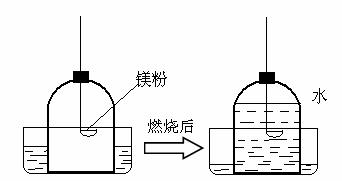
(3)小张同学利用实验室现有的药品红磷和镁粉,利用下列钟罩进行实验,燃烧完毕冷却后的结果如图2,写出红磷在钟罩内燃烧的化学方程式 .
(4)如果实验仪器气密性良好,所用的红磷、镁粉都是足量的,根据实验结果,推测可能的原因,红磷后燃烧后水进入约占
的原因是 .镁粉燃烧后水几乎占满整个钟罩的原因是 .
| 1 |
| 5 |

(1)拉瓦锡在观察到汞面浮起红色渣滓后,还继续加热12天,至红色渣滓不再增加,这样做的理由是
(2)拉瓦锡得到的红色渣滓是氧化汞(氧化汞的化合价为+2价),他又将氧化汞加热分解得到氧气,该反应的化学方程式是
(3)小张同学利用实验室现有的药品红磷和镁粉,利用下列钟罩进行实验,燃烧完毕冷却后的结果如图2,写出红磷在钟罩内燃烧的化学方程式
(4)如果实验仪器气密性良好,所用的红磷、镁粉都是足量的,根据实验结果,推测可能的原因,红磷后燃烧后水进入约占
| 1 |
| 5 |
分析:(1)根据汞与氧气反应生成了氧化汞分析;
(2)根据氧化汞加热分解的反应写出方程式;
(3)根据红磷燃烧的反应写出方程式;
(4)根据红磷燃烧生成了五氧化二磷,镁不仅与氧气反应还能与空气中的其他成分反应分析.
(2)根据氧化汞加热分解的反应写出方程式;
(3)根据红磷燃烧的反应写出方程式;
(4)根据红磷燃烧生成了五氧化二磷,镁不仅与氧气反应还能与空气中的其他成分反应分析.
解答:解:(1)汞与氧气反应生成了红色的氧化汞,持续加热至红色渣滓不再增加,这样做的理由是:确保氧气完全被消耗.
(2)氧化汞加热分解得到氧气和汞,该反应的化学方程式是:2HgO
2Hg+O2↑.
(3)红磷燃烧生成了五氧化二磷,反应的化学方程式:4P+5O2
2P2O5.
(4)由于红磷燃烧消耗了氧气,生成了五氧化二磷固体,瓶中压强减小,所以,红磷后燃烧后水进入约占
;
镁不仅与氧气反应还能与空气中的其他成分反应.所以,镁粉燃烧后水几乎占满整个钟罩.
故答为:(1)确保氧气完全被消耗.(2)2HgO
2Hg+O2↑.(3)4P+5O2
2P2O5.(4)由于红磷燃烧消耗了氧气,生成了五氧化二磷固体,瓶中压强减小;镁不仅与氧气反应还能与空气中的其他成分反应.
(2)氧化汞加热分解得到氧气和汞,该反应的化学方程式是:2HgO
| ||
(3)红磷燃烧生成了五氧化二磷,反应的化学方程式:4P+5O2
| ||
(4)由于红磷燃烧消耗了氧气,生成了五氧化二磷固体,瓶中压强减小,所以,红磷后燃烧后水进入约占
| 1 |
| 5 |
镁不仅与氧气反应还能与空气中的其他成分反应.所以,镁粉燃烧后水几乎占满整个钟罩.
故答为:(1)确保氧气完全被消耗.(2)2HgO
| ||
| ||
点评:本题主要是通过实验探究了空气中氧气的体积分数,掌握汞、磷、镁的化学性质是解答本题的关键.

练习册系列答案
相关题目
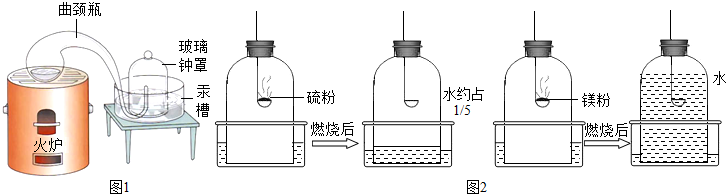
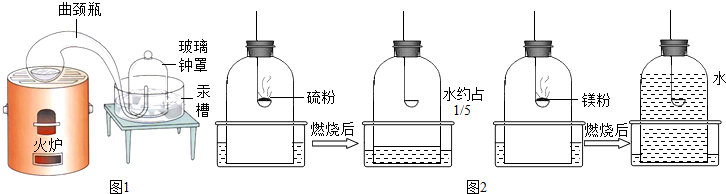
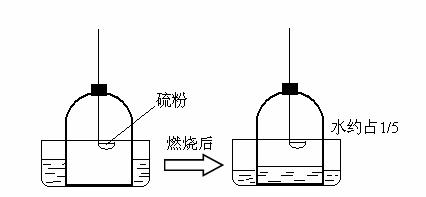 ③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图:
③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图: